在相同条件下,下列各组气体中,分子数一定相同的是( )
| A.14g N2和32g O2 | B.34g NH3和4g H2 |
| C.2L CO2和2L H2O | D.11.2L O2和0.5mol O2 |
下列事实能用勒夏特列原理来解释的是
| A.实验室采用排饱和食盐水的方法收集Cl2 |
| B.500℃左右的温度比室温更有利于合成氨反应 |
| C.H2、I2、HI平衡混合气体加压后颜色加深 |
| D.SO2氧化为SO3,往往需要使用催化剂 |
为探究锌与稀硫酸的反应速率[以v(H2)表示],向反应混合物中加入某些物质,下列判断不正确的是
| A.加入少量NaCl固体,v(H2)不变 | B.加入少量水,v(H2)减小 |
| C.加入少量CH3COONa固体,v(H2)不变 | D.加入少量CuSO4溶液,v(H2)变大 |
已知H2(g)+Br2(l)="2HBr(g)" △H= -72kJ·mol-1,蒸发1mol Br2(l)需要吸收的能量为30kJ,断裂1mol气态H2、Br2、HBr分子内的化学键分别需要吸收的能量为436kJ、akJ、369kJ,则数据a为
| A.404 | B.260 | C.230 | D.200 |
已知101KPa时辛烷的标准燃烧热为—5518kJ·mol-1,含20gNaOH的稀溶液与稀盐酸充分反应放出热量28.7kJ,则下列热化学方程式书写正确的是
①C8H18(l)+ 25/2O2(g)= 8CO2(g)+ 9H2O(g); △H = +5518 kJ·mol-1
②C8H18(l)+ 25/2O2(g)= 8CO2(g)+ 9H2O(l); △H = -5518 kJ·mol-1
③H+(aq)+ OH-(aq)= H2O(l); △H = -57.4 kJ·mol-1
④HCl (aq) + NaOH(aq) =NaCl(aq) + H2O(l); △H = —28.7 kJ·mol-1
| A.①③ | B.②③ | C.②④ | D.② |
反应A(g)+3B(g)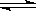 2C(g)的能量变化如图所示,
2C(g)的能量变化如图所示,
结合图像分析下列说法,其中正确的是
| A.若升高温度,则平衡常数增大 |
| B.该反应的焓变为b-a |
| C.达到平衡后,增大压强,平衡逆移 |
| D.催化剂不影响反应的焓变,影响反应的活化能 |