a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种。已知
(1)a、c均能与稀硫酸反应放出气体 (2)b与d 的硝酸盐反应,置换出单质d
(3)c与强碱反应放出气体 (4)c、e在冷浓硝酸中发生钝化,
由此判断a、b、c、d、e分别是
| A.Fe、 Cu、Al、Ag、Mg | B.Al、Cu、Mg 、Ag、Fe |
| C.Mg、 Cu、Al、Ag、Fe | D.Mg 、Ag、Al、Cu、Fe |
X、Y、Z三种元素的原子,其最外层电子排布为ns1,3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是
| A.X2YZ3 | B.X2YZ2 | C.X3YZ3 | D.XYZ3 |
下列叙述中,正确的是
| A.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子 |
| B.在一个基态多电子的原子中,不可能有两个能量完全相同的电子 |
| C.在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高 |
D.某基态原子错误的核外电子排布图为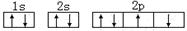 该排布图违背了泡利原理 该排布图违背了泡利原理 |
下列有关化学用语正确的是
| A.Fe的价层电子排布式是:3d64s2 |
B.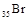 的电子排布式可简写为 的电子排布式可简写为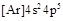 |
C.NH4Cl的电子式为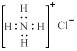 |
D.氯离子结构示意图为: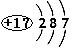 |
某有机物在氧气中充分燃烧,生成的水蒸气和二氧化碳的物质的量之比为1:1,由此可以得出的结论是
| A.该有机物分子中C:H:O原子个数比为1:2:1 |
| B.分子中C:H原子个数比为1:2 |
| C.有机物必定含O元素 |
| D.无法判断有机物是否含O 元素 |
下列反应中,属于取代反应的是
A. CH3CH=CH2+Br2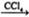 CH3CHBrCH2Br CH3CHBrCH2Br |
B. CH3CH2OH 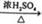 CH2=CH2+H2O CH2=CH2+H2O |
C. CH3COOH+CH3CH2OH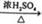 CH3COOCH2CH3+H2O CH3COOCH2CH3+H2O |
D. C6H6+HNO3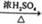 C6H5NO2+H2O C6H5NO2+H2O |