镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图。反应中镁和铝的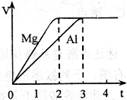
| A.转移电子数之比为2︰3 | B.摩尔质量之比为2︰3 |
| C.物质的量之比为3︰2 | D.反应速率之比为2︰3 |
下列各组物质,按强电解质、弱电解质、非电解质的顺序排列的是
| A.NaCl、BaSO4 、SO2 | B.Cu、CH3C00H、酒精 |
| C.氯化钠晶体、水、酒精 | D.KNO3、NH3·H2O、CaCO3 |
为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格。
| 实 验 目 的 |
试剂及方法 |
| 证明Na2CO3溶液具有碱性 |
|
| 鉴别Na2SO4溶液和(NH4)2SO4溶液 |
|
| 检验自来水中是否含有Cl— |
|
| 除去FeCl2溶液中少量的FeCl3 |
供选择的化学试剂及实验方法
A.加入足量铁粉,过滤
B.滴加酚酞试液,观察现象
C.加稀HNO3和AgNO3溶液,观察现象
D.加入NaOH浓溶液加热,观察现象
化学与生活息息相关,下列做法不正确的是
| A.将废旧电池集中统一处理以防止重金属污染 |
| B.对垃圾进行分类投放、分类回收、分类处理与再利用 |
| C.用甲醛的水溶液浸泡海产品,防腐保鲜 |
| D.按食品卫生标准严格控制食品添加剂(防腐剂等)的用量 |
以下实验操作正确的是
| A.用量筒量取5.0 mL浓硫酸并直接在量筒中稀释 |
| B.用嘴吹灭燃着的酒精灯火焰 |
| C.称量NaOH固体时,将药品直接放在托盘上 |
| D.给烧瓶里的液体加热时,垫上石棉网 |
下列做法不能达到实验目的的是
| A.用灼烧的方法鉴别羊毛和纯棉织品 | B.用氯化钡溶液鉴别盐酸和稀硫酸 |
| C.观察气体颜色区别氮气和氧气 | D.利用丁达尔效应区别溶液和胶体 |