已知:合成氨反应为N2+3H2 2NH3(正反应为放热反应),分析下列问题:
2NH3(正反应为放热反应),分析下列问题:
(1)在一定温度时,可用图中哪一条曲线表示反应物的转化率和压强之间的关系 (填“I”“II”“III”)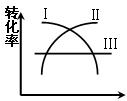
(2)在不同温度和压强下(P1>P2),合成氨反应达到平衡时,混合气体中氨气的体积分数Z%
随温度变化的曲线应为 (填“A”“B”“C”“D”)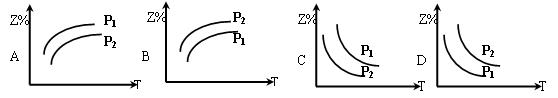
(3)将N2和H2按1:3的体积比通入合成塔,反应达平衡后,NH3的体积分数为20%,则达到平衡时,N2和H2的转化率之比α(N2)∶α (H2)= ;平衡时N2的转化率为_________;平衡混合气体中,n(N2)∶n(H2)∶n(NH3) =
相对分子质量为72的烷烃,其分子式是____,若此有机物的一氯代物分子中有两个—CH3,两个—CH2—,一个  和一个—Cl,它的可能结构分别是____ 、 ____ 、 ____ 、 ____ 。
和一个—Cl,它的可能结构分别是____ 、 ____ 、 ____ 、 ____ 。
有机物:
(1)该物质苯环上一氯代物有________种;
(2)1 mol该物质和溴水混合,耗Br2的物质的量为________________________mol;
(3)1 mol该物质和H2加成最多需H2________mol;
(4)下列说法不对的是________(填字母序号)。
| A.此物质可发生加成、取代、加聚、氧化等反应 |
| B.和甲苯属于同系物 |
| C.使溴水褪色的原理与乙烯相同 |
| D.能使酸性KMnO4溶液褪色发生的是加成反应 |
有X、Y、Z 3种元素,X是有机化合物中必含的元素,Y是地壳里含量最多的元素,Z是质量最轻的元素。X与Y能结合成两种化合物A和B,A可以燃烧,B不可以燃烧,也不支持燃烧;X与Z结合的最简单的化合物C有可燃性;X、Y与Z三种元素结合的化合物D常用作实验室加热的燃料,D被酸性高锰酸钾氧化生成E。
(1)试判断X、Y、Z分别是(填元素符号):X________,Y________,Z________。
(2)试判断A、B、C、D、E各是什么物质(用化学式表示):
A______________,B___________,C__________,D__________,E______________。
(3)完成化学方程式
①C燃烧的化学方程式: _________________________________________。
②D在铜作催化剂且加热条件下与氧气反应的化学方程式:
________________________________________________________________________。
③D与E在浓H2SO4作催化剂、加热条件下反应的化学方程式:
________________________________________________________________________。
已知有机分子中同一碳原子上接两个羟基是不稳定的,会自动脱水: 。
。
醇的氧化是醇的一个重要化学性质。请回答下列醇氧化的有关问题:
(1)乙醇在铜或银催化下受热和氧气反应的化学方程式:
_________________________________________________________。
(2)有人提出了醇氧化的两种可能过程:
①去氢氧化: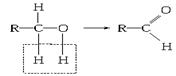
②加氧氧化: (在方框中填写有机物结构简式,说明加氧氧化)。
(在方框中填写有机物结构简式,说明加氧氧化)。
(3)若要证明这两种过程哪一种是正确的,你准备用的方法是________________(回答方法名称即可)。
(9分)A、B、C、D、E五种有机物,它们分子中C、H、O三种元素的质量比都是6∶1∶8。在通常状况下,A是一种有刺激性气味的气体,对氢气的相对密度为15,其水溶液能发生银镜反应。B的相对分子质量是A的6倍,C和B是同分异构体,两物质都是具有甜味的白色晶体,但B常用作制镜工业的还原剂。D和E两物质的蒸气密度都是2.68 g/L(标准状况下),它们互为同分异构体,但D的水溶液能使石蕊试液变红,而E是不溶于水的油状液体,具有水果香味。试写出A、B、C、D、E的名称和A、B、D、E的结构简式:
A.________________________,______________________________;
B.________________________,______________________________;
C.________________________;
D.________________________,_____________________________;
E.________________________,______________________________。