某学生设计如下实验装置利用氯气与消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题: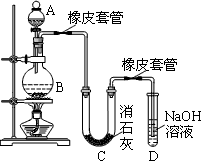
(1)A仪器的名称是 ,所盛试剂是 。
(2)漂白粉将在U型管中产生,其化学反应方程式是 。
(3)有同学建议在两个橡皮套管内的玻璃管口应尽量紧靠,原因是 。
(4)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现主要原因是在U型管中存在两个副反应:①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,此副反应的化学方程式为: ,为避免此副反应的发生,可采取的措施是 。
②写出另一个副反应的化学方程式 。为避免此副反应发生,可采取的措施是 。
(5)在空气中,漂白粉会失效,原因是(用方程式表示) 。
下列说法或表示法正确的是
| A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.由C(石墨)→C(金刚石) ΔH =" +119" kJ·mol—1可知,金刚石比石墨稳定 |
| C.在稀溶液中:H++OH-===H2O ΔH = -57.3 kJ· mol—1,若将含1mol CH3COOH的醋酸溶液与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ |
| D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+ O2(g)==2H2O(l) ΔH =" +285.8" kJ· mol—1 |
已知(1)H2O(g)==H2O(l) ΔH1=-Q1 kJ·mol-1
(2)CH3OH(g)==CH3OH(l)△H2=-Q2 kJ·mol-1
(3)2CH3OH(g) +3O2(g) ==2CO2(g)+4H2O(g)△H3=-Q3 kJ·mol-1
(Q1、Q2、Q3均大于0)若要使32g液态甲醇完全燃烧,最后恢复到室温,放出的热量为(单位:kJ)()
| A.Q1+Q2+Q3 | B.0.5 Q3-Q2+2Q1 | C.0.5 Q3+ Q2-2Q1 | D.0.5(Q1+Q2+Q3) |
下列说法中正确的是()
| A.需加热才能发生的反应一定是吸热反应 |
| B.任何放热反应在常温条件一定能发生反应 |
| C.反应物和生成物分别具有的总能量决定了反应是放热反应还是吸热反应 |
| D.ΔH的大小与热化学方程式的计量系数无关 |
25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是()
| A.C(s)+1/2 O2(g)=CO(g)△H=" ―393.5" kJ/mol |
| B.2H2(g)+O2(g)=2H2O(l)△H="" +571.6 kJ/mol |
| C.CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=" ―890.3" kJ/mol |
| D.C6H12O6(s) +6O2(g)=6CO2(g)+6H2O(l)△H=" ―2800" kJ/mol |
对于可逆反应:2A(g)+B(g)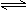 2C(g)△H<0,下列各图正确的是()
2C(g)△H<0,下列各图正确的是()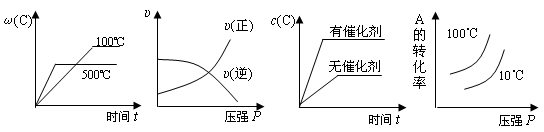
A B C D