制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应实现:
①Si(s)+3HCl(g) SiHCl3(g)+H2(g);ΔH="-381" kJ·mol-1
SiHCl3(g)+H2(g);ΔH="-381" kJ·mol-1
②SiHCl3+H2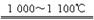 Si+3HCl 对上述两个反应的叙述中,错误的是
Si+3HCl 对上述两个反应的叙述中,错误的是
| A.两个反应都是置换反应 | B.反应②是吸热反应 |
| C.两个反应互为可逆反应 | D.两个反应都是氧化还原反应 |
用石墨为电极材料电解时,下列说法正确的是
| A.电解NaOH溶液时,溶液浓度将减小,pH不变 |
| B.电解H2SO4溶液时,溶液浓度将增大,pH不变 |
| C.电解Na2SO4溶液时,溶液浓度将增大,pH不变 |
| D.电解NaCl溶液时,溶液浓度将减小,pH不变 |
X、Y、Z、M代表四种金属元素。金属X和Z用导线连接放入稀硫酸中时,Z极上有H2放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为
| A.X>Z>Y>M | B.X>Y>Z>M | C.M>Z>X>Y | D.X>Z>M>Y |
关于电解NaCl水溶液,下列叙述正确的是
| A.电解时在阳极得到氯气,在阴极得到金属钠 |
| B.若在阳极附近的溶液中滴入KI试液,溶液呈棕色 |
| C.若在阴极附近的溶液中滴入酚酞试液,溶液呈无色 |
| D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性 |
关于如图所示装置的叙述,正确的是 
| A.铜是阳极,铜片上有气泡产生 | B.铜片质量逐渐减少 |
| C.电流从锌片经导线流向铜片 | D.铜离子在铜片表面被还原 |
下列关于实验现象的描述不正确的是
| A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B.用锌片做阳极,铁片做做阴极,电解氯化锌溶液,铁片表面出现一层锌 |
| C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |
| D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |