T℃时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是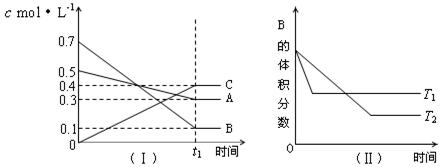
A、在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动
B、(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向逆反应方向移动
C、T℃时,在相同容器中,若由0.3mol·L—1 A,0.1 mol·L—1 B,和0.4 mol·L—1 C反应,达到平衡后C的浓度仍为0.4 mol·L—1
D、其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
在物质的量浓度均为0.01mo l · L-1的CH3COOH和CH3COONa混合液中,测得C(CH3COO-)>c(Na+),则下列关系式正确的是()。
A c(OH-)=c(H+)
B c(OH-)>c(H+)
C c(CH3COOH)>C(CH3COO-)
D c(CH3COOH)+C(CH3COO-)="0.02" mo l · L-1
下列有关实验描述中,正确的是( )
| A.检验溴乙烷中的溴元素:在溴乙烷中滴入氢氧化钾溶液加热后,用稀硝酸酸化再滴加硝酸银溶液 |
| B.测氯水的pH,可用玻璃棒蘸取氯水点在pH试纸上,待其变色后和标准比色卡比较 |
| C.配制一定物质的量浓度溶液时,用量筒量取浓溶液时仰视读数,所得溶液的浓度偏低 |
| D.证明CH2=CHCH2CHO中一定有碳碳不饱和键:滴入KMnO4酸性溶液,看紫红色是否褪去 |
室温下,有下列四种溶液:①0.1mol·L-1氨水,
②0.1mol·L-1 NH4Cl溶液,③0.2mol·L-1盐酸与0.2mol·L-1NH4Cl
溶液等体积混合,④0.2mol·L-1NaOH溶液与0.2mol·L-1氨水等体
积混合,四种溶液中c(NH )由大到小排列正确的是()
)由大到小排列正确的是()
| A.②③④① | B.④①②③ | C.①④②③ | D.③②①④ |
在25℃浓度均为1mo l · L-1的(NH4)2SO4, (NH4)2Fe(SO4)2,(NH4)2CO3溶液中,测得c(NH4+)分别为a,b,c (单位mo l · L-1)则下列关系式正确的是( ).
A a=b=c
B a>b>c
C a>c>b
D b>a>c
在0.1mol·L-1的Na2CO3溶液中下列关系式正确的是( ).
A c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
B c(OH-)=c(H+)+c(HCO3-)
C c(OH-)=c(H+)+2c(H2CO3)
D c(OH-)=c(H+)+c(HCO3-)+c(H2CO3)