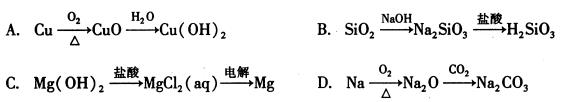在配制一定物质的量浓度的盐酸时,下列错误操作可使所配制溶液的浓度偏高的是
( )
| A.用量筒量取浓盐酸时俯视量筒刻度进行读数 |
| B.溶解搅拌时有液体飞溅 |
C.定容时俯视容量瓶瓶颈刻度线 |
| D.摇匀后见液面下降,再加水至刻度线 |
下列图示与对应的叙述相符的是
| A.图甲表示催化剂能改变化学反应的焓变 |
| B.图乙表示向氨水中加水时溶液导电性的变化情况,且溶液c(OH—)大小:a<b |
C.由图丙可知反应2A(g)+B(g)  C(g)的△H >O,且 a=2 C(g)的△H >O,且 a=2 |
| D.图丁表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化情况 |
一种微生物燃料电池的结构示意图如下所示,关于该电池的叙述正确的是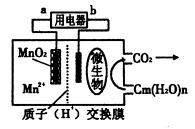
| A.电池工作时,电子由a流向b |
| B.微生物所在电极区放电时发生还原反应 |
| C.放电过程中,H+从正极区移向负极区 |
| D.正极反应式为:MnO2+4H+ +2e— ===Mn2+ +2 H2O |
下列相关工业制法的描述不正确的是
| A.电解熔融氯化钠制取金属钠 |
| B.电解熔融的Al(OH) 3制取金属铝 |
| C.用石英、纯碱、石灰石为原料制玻璃 |
| D.用焦炭在电炉中还原二氧化硅得到含杂质的粗硅 |
利用下列图示进行相应实验,能达到目的的是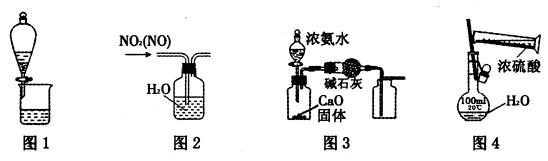
| A.用图1可萃取碘水中的碘 |
| B.用图2可除去NO2中的NO |
| C.用图3制取并收集干燥纯净的NH3 |
| D.用图4配制100mL一定物质的量浓度的稀硫酸 |
下列物质间的转化在给定条件下能实现的是