根据以下3个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H=Q1 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(l) △H=Q2 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(g) △H=Q3 kJ/mol
判断Q1、Q2、Q3三者关系正确的是( )
| A.Q1>Q2>Q3 | B.Q1>Q3>Q2 | C.Q3>Q2>Q1 | D.Q2>Q1>Q3 |
可以证明某化合物一定含有离子键的性质是
| A.具有较高的熔点 | B.熔融状态能导电 |
| C.可溶于水 | D.溶于水能导电 |
如图是氩元素在元素周期表中的具体信息。其中39.95是
| A.氩的原子序数 | B.氩原子的质量数 |
| C.氩元素的相对原子质量 | D.氩原子的相对原子质量 |
新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源的是
| A.石油 | B.太阳能 | C.煤 | D.天然气 |
提出元素周期律并绘制了第一个元素周期表的科学家是
| A.戴维 | B.阿伏加德罗 | C.门捷列夫 | D.道尔顿 |
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得: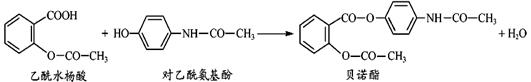
下列有关叙述正确的是
| A.贝诺酯分子中有三种含氧官能团 |
| B.可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚 |
| C.乙酰水杨酸和对乙酰氨基酚均能与Na2CO3溶液反应 |
| D.贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚 |