某课外小组利用H2还原CuO粉末测定铜元素的相对原子质量,下图是测定装置的示意图,A中的试剂是盐酸,C中试剂是稀氢氧化钠溶液。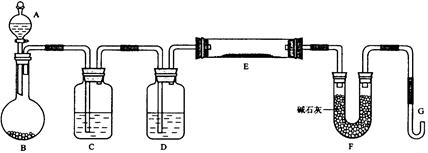
请回答下列问题。
(1)仪器中装入的试剂:B 、D 。
(2)装置C的作用是 。
(3)连接好装置后应首先 。
(4)“①加热反应管E”和“②从A瓶逐滴滴加液体”这两步操作应该先进行的是 (填序号)。在这两步之间还应进行的操作是 。
(5)反应过程中G管逸出的气体是 ,其处理方法是 。
(6)从实验中测得了下列数据:
①空E管的质量a;②E管和CuO的总质量b;
③反应后E管和Cu粉的总质量c(冷却到室温称量);
④反应前F管及内盛物的总质量d;⑤反应后F管及内盛物的总质量e。
由以上数据可以列出计算Cu的相对原子质量的两个不同计算式(除Cu外,其他涉及的元素的相对原子质量均为已知):
计算式1:Ar(Cu)= ;计算式2:Ar(Cu )= 。
三氯化铁是一种很重要的铁盐,主要用于污水处理,具有效果好、价格便宜等优点。工业上可将铁屑溶于盐酸中,先生成FeCl2,再通入Cl2氧化来制备FeCl3溶液。
(1)将标准状况下的a L氯化氢气体溶于100 g水中,得到的盐酸的密度为b g·mL-1,则该盐酸的物质的量的浓度是________。
(2)向100 mL的FeBr2溶液中通入标准状况下Cl2 3.36 L,反应后的溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为________。
(3)FeCl3溶液可以用来净水,其净水的原理为______________________________________(用离子方程式表示),若100mL 2mol·L-1的FeCl3溶液净水时,生成具有净水作用的微粒数________0.2NA(填“大于”、“等于”或“小于”)。
二硫化亚铁是Li/FeS2电池的正极活性物质,可用水热法合成。FeSO4、Na2S2O3、S及H2O在200 ℃连续反应24 h,四种物质以等物质的量反应,再依次用CS2、H2O洗涤、干燥及晶化后得到。
(1)合成FeS2的离子方程式为_____________________________________。
(2)用水洗涤时,如何证明SO42—已除尽?________________________________________。
(3)已知1.20 g FeS2在O2中完全燃烧生成Fe2O3和SO2气体放出8.52 kJ热量,FeS2燃烧反应的热化学方程式为__________________________。
(4)取上述制得的正极材料1.120 0 g(假定只含FeS一种杂质),在足量的氧气流中充分加热,最后得0.800 0 g红棕色固体,试计算该正极材料中FeS2的质量分数(写出计算过程)。
分类思想以及用分类思想研究一类物质的通性和特殊性是学习化学的一种重要思维方式和手段。以下是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学的知识,按要求填空:
(1)上述第一级分类标准(分成A、B组的依据)是____________________。
(2)F组中物质除了Cl2外还有________(填化学式)。
(3)D组中的氨水呈弱碱性,用电离方程式表示其呈弱碱性的原因:
______________________________________________________________。
(4)由Al3+制备Al(OH)3,最好不选择D组中的NaOH溶液,用离子方程式说明理由:_______________________________________________________。
(5)FeCl3的水溶液滴入沸水可得到以Fe(OH)3为分散质的红褐色胶体
①该红褐色胶体中Z(OH)3粒子的直径大小范围是______________。
②FeCl3溶液滴入沸水可得到Fe(OH)3红褐色胶体的反应的离子方程式是____________________________。
下面是有关物质的转化关系图(部分产物已省略),其中A为单质,E在常温下为液体,D是一种温室气体,C的相对分子质量为78。请回答相关问题。
(1)下列对C的结构、性质推断中不正确的是 ( )。
| A.久置于空气中会变成白色 | B.具有强氧化性 |
| C.晶体中存在离子键与非极性键 | D.是一种碱性氧化物 |
(2)A的原子结构示意图为____________________,H的电子式为____________________,E的结构式为____________________。
(3)C和E反应生成H的离子方程式为__________________,反应中氧化剂与还原剂的物质的量之比为______。
硅及其化合物对人类现代文明的发展具有特殊贡献。请回答下列有关问题:
(1)硅原子的结构示意图:________。
(2)下列物品或设备所用的材料属于硅酸盐的是________。
①长江三峡水泥大坝 ②石英光导纤维 ③陶瓷坩埚
④普通玻璃 ⑤硅太阳能电池
| A.①②⑤ | B.③④⑤ | C.②③④ | D.①③④ |
(3)常温下,SiCl4为液态,沸点为57.6 ℃,在空气中冒白雾。制备高纯度硅的中间产物SiCl4中溶有液态杂质,若要得到高纯度SiCl4,应采用的方法是________;用化学方程式及必要文字解释SiCl4在空气中冒白雾的原因:
___________________________________________________________。