某课外小组模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下列仪器来制取氧气并测量氧气的体积。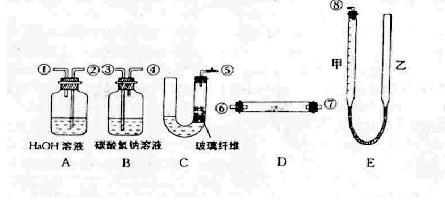
上图中量气装置E是由甲.乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。 甲管有刻度(0-50毫升),供量气用;乙管可上下移动,以调节液面高低。
实验室可供选用的药品还有:稀硫酸.盐酸.过氧化钠.碳酸钠.大理石.水。试回答:
(1)上述装置中与制取氢气所用装置原理相似的是(填各装置的字母):
(2上述装置的连接顺序是(填各接口的编号,其中连接胶管及夹持装置均省略):
(3)装置C中放入的反应物是 和
(4)装置A的作用是 装置B的作用是
(5)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数、求其差值的过程中,应注意:
a.
b.
可逆反应A(g)+3B(g) 2C(g)+2D(g),在不同条件下的反应速率如下,其中反应速率最快的是 ()
2C(g)+2D(g),在不同条件下的反应速率如下,其中反应速率最快的是 ()
| A.vB ="0.6mol/" ( L·s) | B.vA="0.5mol/" (L·s) |
| C.vc="0.4mol/" ( L·s) | D.vD="0.45mol/" (L·s) |
下列说法正确的是 ( )
| A.在101 kPa、25 ℃时,中和热为57.3 kJ/mol,则表示Ba(OH)2的稀溶液与足量稀硫酸反应的热化学方程式为: Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l)ΔH=-114.6 kJ/mol |
B.在101 kPa、25 ℃时,2 g H2完全燃烧生成液态水,放出285.8 kJ的热量;则表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l)ΔH=-285.8 kJ/mo l l |
| C.强电解质都是离子化合物,弱电解质都是共价化合物。 |
| D.在相同情况下,强电解质溶液的导电性比相同浓度弱电解质溶液的导电性强 |
强电解质和弱电解质的本质区别是()
| A.导电能力 | B.相对分子质量 | C.电离程度 | D.溶解 |
关于有效碰撞理论,下列说法正 确的是()
确的是()
| A.活化分子间所发生的所有碰撞为有效碰撞 |
| B.增大反应物浓度能够增大活化分子百分数,化学反应速率一定增大 |
| C.升高温度,活化分子百分数增加,化学反应速率一定增大 |
| D.增大压强,活化分子数一定增加,化学反应速率一定增大 |
下列与化学反应能量变化相关的叙述正确的是 ( )
| A.生成物能量一定低于反应物总能量 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |