某同学用胆矾晶体(CuSO4·5H2O )配制0.40mol/L的CuSO4溶液1000mL,
回答下列问题:
(1)所需仪器为:(1000mL)容量瓶、托盘天平、药匙、 胶头滴管 ,还需要哪些玻璃仪器才能完成该实验,请写出:①___________ ,②___________
(2)写出该实验步骤 ①计算 ②称量胆矾__________g ③ ___________ ④转移 ⑤洗涤并转移 ⑥定容 ⑦摇匀
(3)下列情况对所配制的CuSO4溶液浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.容量瓶用蒸馏洗涤后残留有少量的水________________
B.所用过的烧杯、玻璃棒未洗涤________________
C.定容时俯视刻度线________________
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:
①X元素原子价电子排布式为ns2np2,且原子半径是同族元素中最小的。
②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电
子排布中,p轨道上只有1个未成对电子。
③Z+与Y 2-具有相同的电子层结构;
请回答:
(1)Z2Y2的电子式为,含有的化学键类型为,Z2Y2为晶体。
(2)X、Y、Z三种元素所形成的常见化合物的名称为;XY2的结构式为,分子的立体构型为。
(3)X、Y、Z、W四种元素所形成的单质中,熔点最高、硬度最大的是(填名称);晶体ZW的熔点比晶体XW4明显高的原因是。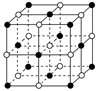
(4)ZW晶体的结构示意图如图。已知:ZW晶体的密度为ρ,摩尔质量为M,阿伏伽德罗常数为NA,则ZW晶体中两个最近的Z离子中心间的距离d可以表示为d=。
下表为元素周期表的一部分,a、b、c…为元素周期表中前4周期的部分元素。
回答下列问题:
| a |
|||||||||||||||||
| e |
f |
g |
|||||||||||||||
| b |
hh |
||||||||||||||||
| c |
d |
[ |
d |
||||||||||||||
(1)d3+的未成对电子数为个;
(2)请比较e、f、g三种元素的第一电离能由大到小的顺序(写元素符号)
(3)请写出h元素原子价电子轨道表示式;
(4)ea3分子的电子式是,其分子的空间构型是,分子中e原子的杂化类型是。
氮是地球上极为丰富的元素。
(1)Li3N晶体中氮以N3-存在,基态N3-的核外电子排布式为。
(2)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是,与同一个N3-相连的X+有个。
(1)A元素的负一价离子和B元素的正一价离子的电子层结构都与氩相同,A的离子结构示意图为,B元素名称为;
(2)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,C的元素基态原子的外围电子排布式为.
(3)D元素的原子序数为33,该元素原子的核外电子共有种不同的运动状态,此元素原子的核外电子排布式是
(4)N≡N的键能为942kJ·mol-1,N—N单键的键能为247kJ·mol-1,通过计算说明N2中的键更稳定(填“σ”或“π”)。
(5)下列4种物质熔、沸点由高到低排列为(填序号).
①金刚石②晶体锗③晶体硅④金刚砂
【化学——有机化学基础】
利胆解痉药“亮菌甲素”跟(CH3)2SO4反应生成A。二者的结构简式如图。

试回答:
(1)“亮菌甲素”的分子式为__________________,1 mol“亮菌甲素”跟浓溴水反应时最多消耗___________molBr2;A不能发生的化学反应有_________________。
① 加成反应 ② 酯化反应 ③ 水解反应 ④ 消去反应
(2)有机物A能发生如下转化。 提示:


① C→D的化学方程式为__________________________________________________。
② 1 molG跟1 mol H2在一定条件下反应,生成物的结构简式为。
③ 符合下列条件的E的同分异构体有_________种,写出其中任意一种的结构简式。
a. 遇FeCl3溶液呈紫色 b. 不能发生水解反应,能发生银镜反应
c. 苯环上的一氯取代物只有一种,分子中无甲基
_____________________________________________________________________。