下列离子方程式书写不正确的是
| A.在氢氧化钡溶液中逐滴加入硫酸氢钠溶液至恰好呈中性: Ba2++2OH-+2H++SO42-====BaSO4↓+2H2O |
| B.在苯酚钠溶液中通入少量二氧化碳:C6H5O-+H2O+CO2→C6H5OH+HCO3- |
| C.在澄清石灰水中滴加过量碳酸氢钠溶液: Ca2++2HCO3-+2OH-====CaCO3↓+2H2O+ CO32- |
| D.向100mL0.2mol/L溴化亚铁的溶液中慢慢通入448mL(标准状况)Cl2: |
2Fe2++4Br-+3Cl2====2Fe3++2Br2+6Cl-
设NA为阿伏加德罗常数,下列说法正确的是
| A.23 g钠在氧气中完全燃烧失电子数为0.5NA |
| B.46gNO2和N2O4混合气体中含有氮原子数为1NA~2NA |
| C.标准状况下,11.2L的SO3所含分子数为0.5 NA |
| D.室温下,16g甲烷含有共价键数为4 NA |
分类方法在化学学科的发展中起到重要的作用。下列分类标准合理的是
| A.根据纯净物的元素组成,将纯净物分为单质和化合物 |
| B.根据溶液导电能力强弱,将电解质分为强电解质、弱电解质 |
| C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| D.根据反应中的能量变化,将化学反应分为“化合、分解、复分解、置换”四类 |
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧
瓶内的气体接触(如图),容器内的压强由大到小的顺序是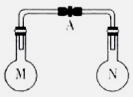
| 编号 |
① |
② |
③ |
④ |
| 气体M |
H2S |
H2 |
N H3 |
NO |
| 气体N |
SO2 |
Cl2 |
HCl |
O2 |
A.①②③④ B.②④①③ C.④①②③ D.①④③②
下列表中对于相关物质的分类全部正确的一组是
| 编号 |
纯净物 |
混合物 |
弱电解质 |
非电解质 |
| A |
明矾 |
蔗糖 |
NaHCO3 |
CO2 |
| B |
天然橡胶 |
石膏 |
SO2 |
CH3CH2OH |
| C |
冰 |
王水 |
H2SiO3 |
Cl2 |
| D |
胆矾 |
玻璃 |
H2CO3 |
NH3 |
关于胶体和溶液的区别,下列叙述中正确的是
| A.溶液呈电中性,胶体带有电荷 |
| B.溶液中溶质微粒一定不带电,胶体中分散质微粒带有电荷 |
| C.溶液中分散质微粒能透过滤纸,胶体中分散质微粒不能透过滤纸 |
| D.溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现明亮的光带 |