下列各项操作中,能发生“先沉淀后溶解”现象的是 ( )
| A.向饱和Na2CO3溶液中通入过量的CO2 |
| B.向Fe(OH)3胶体中逐滴滴入过量的稀H2SO4 |
| C.向AlCl3溶液中通入过量的NH3 |
| D.向CaCl2溶液中通入过量的CO2 |
除去NaCl固体中少量泥沙,肯定不会涉及的操作是( )
| A.蒸馏 | B.溶解 | C.搅拌 | D.过滤 |
某有机物的结构简式为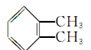 ,下列命名正确的是()
,下列命名正确的是()
| A.邻二甲苯 | B.1,6二甲苯 | C.1,2二甲苯 | D.乙苯 |
某烯烃与氢气加成后得到2,2-二甲基戊烷,烯烃的名称是()
| A.2,2-二甲基-3-戊烯 | B.2,2-二甲基-4-戊烯 |
| C.4,4-二甲基-2-戊烯 | D.2,2-二甲基-2-戊烯 |
根据有机化合物的命名原则,下列命名正确的是()
A.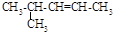 2-甲基-3-戊烯 2-甲基-3-戊烯 |
B.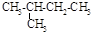 异丁烷 异丁烷 |
| C.CH3CH(C2H5)CH2CH2CH32-乙基戊烷 |
| D.CH3CH(NO2)CH2COOH 3-硝基丁酸 |
下列用系统命名法命名的有机物名称正确的是()
| A.2-甲基-4-乙基戊烷 | B.3,4,4-三甲基己烷 |
| C.1,2,4-三甲基-1-丁醇 | D.2,3-二乙基-1-戊烯 |