某溶液中只可 能含有下列离子中的
能含有下列离子中的 几种:K+、NH4+、NO3-、SO42- 、SO32- 、CO32 -取200mL该溶液分成两等份,进行以下实验:
几种:K+、NH4+、NO3-、SO42- 、SO32- 、CO32 -取200mL该溶液分成两等份,进行以下实验:
(1)第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL。
(2)第二份先加足量的盐酸无现象,再加足量的BaCl2,得到2.33g固体,则该溶液中( )
| A.可能含有K+、CO32 - | B.肯定含有NO3-、SO42 -、NH4+ |
| C.一定不含有NO3- | D.一定含有K+且c(K+)≥ 0.1mol/L |
下列说法正确的是
| A.过滤时漏斗下端与烧杯内壁要保持接触,分液时分液漏斗下端与锥形瓶(或烧杯)内壁不能接触 |
| B.受强酸或强碱腐蚀致伤时,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗,并视情况作进一步处理 |
| C.比较去锈的铁钉和去锈的绕有细铜丝的铁钉与同浓度的盐酸反应速率快慢时,可以加K3[Fe(CN)6]溶液,观察铁钉周围出现蓝色沉淀的快慢 |
| D.自来水厂常用某些含铝或铁的化合物作净水剂,是由于这些物质具有杀菌消毒作用 |
下列说法正确的是
| A.生物质能来源于植物及其加工产品所贮存的能量,绿色植物通过光合作用将化学能转化为生物质能 |
| B.人们利用元素周期律在过渡元素中寻找各种性能优良的催化剂,以降低化学反应的活化能,从而起到很好的节能效果 |
| C.合成氨反应在低温下能够自发进行,是因为反应物键能之和大于生成物键能之和 |
| D.气化、液化和干馏是煤综合利用的主要方法,这三者中只有干馏是化学变化 |
水溶液中可能存在Na+、Al3+、Fe2+、NH4+、NO3-、CO32-、SO42-中的几种离子,且存在的各离子具有相同的物质的量,某同学对该溶液进行如下实验: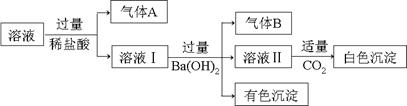
下列判断正确的是
| A.气体A一定是CO2,气体B一定是NH3 |
| B.白色沉淀一定是Al(OH)3 |
| C.溶液中一定存在Al3+、Fe2+、NO3-、NH4+ |
| D.溶液中一定不存在大量Na+ |
取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol·L-1的NaOH溶液或0.10mol·L-1的稀氨水滴定得下图。下列说法正确的是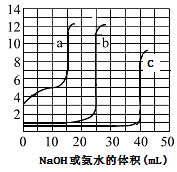
| A.由图可知曲线c为NaOH滴定硫酸 |
| B.由图可知硫酸的物质的量浓度大于盐酸的物质的量浓度 |
| C.曲线b、c的滴定实验可用酚酞做指示剂 |
| D.由图可知滴定前醋酸电离度约为1.67﹪ |
下列叙述正确的是
| A.Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图一所示,石墨电极上产生氢气,铜电极发生氧化反应 |
| B.图一所示当有0.1mol电子转移时,有0.1molCu2O生成 |
| C.图二装置中发生:Cu+2Fe3+ = Cu2++2Fe2+,X极是负极,Y极材料可以是铜 |
| D.如图二,盐桥的作用是传递电荷以维持电荷平衡,Fe3+经过盐桥进入左侧烧杯中 |