已知在1×105Pa、298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化
学方程式正确的是( )
A.H2O(g)=H2(g)+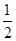 O2(g); O2(g); H= +242kJ·mol-1 H= +242kJ·mol-1 |
B.2H2(g)+O2(g) = 2H2O(l); H= -484kJ·mol-1 H= -484kJ·mol-1 |
C.H2(g)+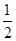 O2(g)=H2O(g); O2(g)=H2O(g); H= +242kJ·mol-1 H= +242kJ·mol-1 |
D.2H2(g)+O2(g)=2H2O(g); H="+" 484kJ·mol-1 H="+" 484kJ·mol-1 |
对于可逆反应mA(g)+nB(g) pC(g)+gD(g),若其它条件都不变,只是在反应前是否加入催化剂,可得到两种υ~t图象如下图:
pC(g)+gD(g),若其它条件都不变,只是在反应前是否加入催化剂,可得到两种υ~t图象如下图: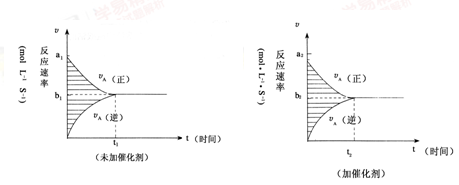
如下关系正确的为 ()
①a1=a2②a1<a2③b1=b2④b1<b2⑤t1>t2⑥t1=t2⑦两图中阴影部分面积相等 ⑧右图阴影部分面积更大
| A.②④⑤⑦ | B.②④⑥⑧ | C.②③⑤⑦ | D.②③⑥⑧ |
在体积一定的密闭容器中给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g) + bB(g) xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指()
xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指()
A.反应物A的百分含量
B.平衡混合气中物质B的百分含量
C.平衡混合气的密度
D.平衡混合气的平均摩尔质量
反应FeO(s)+C(s)=Fe(s)+CO(g);ΔH>0,ΔS>0,下列说法正确的是
| A.低温下自发进行,高温下非自发进行 |
| B.高温下自发进行,低温下非自发进行 |
| C.任何温度下均为非自发进行 |
| D.任何温度下均为自发进行 |
密闭容器中,充入一定量的HI气体,发生反应2HI(g) H2(g)+I2(g);ΔH>0,在t1时达到平衡,t2时加热升温并保温,到t3时又达到新平衡,符合这一变化的图像是
H2(g)+I2(g);ΔH>0,在t1时达到平衡,t2时加热升温并保温,到t3时又达到新平衡,符合这一变化的图像是
在由水电离出的c(H+)=1×10-13 mol·L-1的溶液中一定大量共存的离子组是
| A.Fe2+、Na+、NO3-、 Cl- |
| B.Ba2+、Na+、NO3-、Cl- |
| C.SO42-、S2O32-、NH4+、Na+ |
| D.Mg2+、Na+、Br -、AlO2- |