已知下列热化学方程式:Zn(s)+1/2O2(g)=ZnO(s)ΔH1="—351.1" kJ/mol ;
Hg(l)+1/2O2(g)=HgO(s) ΔH2="—90.7" kJ/mol 。
由此可知Zn(s)+HgO(s)="==" ZnO(s)+Hg(l)△H3。其中△H3的值是 ( )
| A.—441.8kJ/mol | B.—254.6kJ/mol | C.—438.9kJ/mol | D.—260.4kJ/mol |
往浅绿色的Fe(NO3)2溶液中逐滴加入稀盐酸,溶液的颜色变化应该是
| A.颜色变浅 | B.变为绿色 | C.没有改变 | D.变棕黄色 |
在体积可变的密闭容器中,反应mA(气)+nB(固)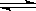 pC(气)达到平衡后,压缩容器的体积,发现A的转化率随之降低。下列说法中,正确的是
pC(气)达到平衡后,压缩容器的体积,发现A的转化率随之降低。下列说法中,正确的是
| A.(m+n)必定小于p | B.(m+n)必定大于p |
| C.m必定小于p | D.n必定大于p |
下列各反应达到化学平衡后,加压或降温都能使化学平衡向逆反应方向移动的是:
A.2NO2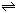 N2O4(正反应为放热反应) N2O4(正反应为放热反应) |
B.C(固)+CO2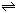 2CO (正反应为吸热反应) 2CO (正反应为吸热反应) |
C.N2+3H2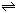 2NH3(正反应为放热反应) 2NH3(正反应为放热反应) |
D.H2S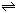 H2+S(固)(正反应为吸热反应) H2+S(固)(正反应为吸热反应) |
一定条件下反应2AB(g)  A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A.单位时间内生成n molA2,同时消耗2n molAB
B.容器内,3种气体AB、A2、B2共存
C.AB的消耗速率等于A2的消耗速率
D.容器中各组分的体积分数不随时间变化
通常情况下,能用浓硫酸干燥且属于非极性分子的气体是
| A.NH3 | B.H2S | C.CO2 | D.SO2 |