下列离子方程式中正确的是 ( )
| A.铜与稀硝酸反应: Cu+2H++NO3-===Cu2++NO↑+H2O |
| B.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液: Fe2++2H++H2O2===Fe3++2H2O |
| C.过量的二氧化碳通入漂白粉溶液中: ClO-+CO2+H2O===HClO+HCO3- |
| D.AlCl3溶液中加入过量氨水: |
Al3++4NH3·H2O===AlO2-+2H2O+4NH4+
有一铁的氧化物样品,用140 mL 5 mol·L-1盐酸可恰好使其完全溶解。所得溶液可吸收标准状况下0.56 L氯气,使其中的Fe2+全部转化为Fe3+。该样品可能的化学式为()
| A.Fe4O5 | B.Fe5O7 | C.Fe2O3 | D.Fe3O4 |
今有NH3、O2、NO2在标准状况下的混合气体20.16L,通过稀硫酸后,溶液质量增加了34.1g,气体缩小至2.24L(标况下),将余烬木条插入其中,木条不复燃,则原混合气NH3、O2、NO2物质的量比为()
| A.1∶1∶7 | B.2∶2∶5 | C.3∶1∶4 | D.5∶2∶2 |
已知X、Y分别为同周期的ⅠA和VIA族的两种元素,它们的原子序数分别为a和b,则下列关系不可能成立的是()
| A.a=b –15 | B.a=b –29 | C.a=b – 9 | D.a=b –5 |
白磷与氧气可发生如下反应:P4+5O2===P4O10。已知断裂下列化学键需要吸收的能量分别为: P—P a kJ·mol-1、P—O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。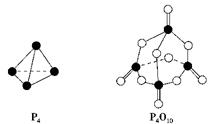
根据下图所示的分子结构和有关数据估算该反应的ΔH,其中正确的是( )
| A.(4c+12b-6a-5d)kJ·mol-1 |
| B.(6a+5d-4c-12b)kJ·mol-1 |
| C.(4c+12b-4a-5d)kJ·mol-1 |
| D.(4a+5d-4c-12b)kJ·mol-1 |
把A、B、C、D四块金属片浸入稀硫酸中,分别用导线两两相连可以组成原电池。A、B相连时A为负极;C、D相连时,电流由D→C;A、C相连时,C极上产生大量气泡,B、D相连时,D极发生氧化反应。这四种金属的活动性顺序是( )
A.A>B>C>DB.A>C>D>BC.C>A>B>D D.B>D>C>A