将等物质的量的X.Y气体充入一个容积可变的密闭容器中,在一定条件下发生如下反应并达到平衡:X(g)+Y(g)+2M(s)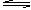 2Z(g);ΔH<0。当改变某个条件并维持新条件直至达到新平衡,下表中关于新平衡与原平衡的比较,正确的是 (
2Z(g);ΔH<0。当改变某个条件并维持新条件直至达到新平衡,下表中关于新平衡与原平衡的比较,正确的是 ( )
)
| 选择 |
改变的条件 |
正.逆反应速率变化 |
新平衡和原平衡比较 |
| A |
升高温度 |
逆反应速率增大量大于正反应速率增大量 |
X的体积分数变大 |
| B |
增大压强 |
正反应速率增大,逆反应速率减小 |
Z的浓度不变 |
| C |
减小压强 |
正.逆反应速率都减小 |
Y的体积分数变大 |
| D |
充入一定量Z |
逆反应速率增大 |
X的体积分数变大 |
某有机物燃烧后产物只有CO2和H2O,可推出的结论是,这种有机物中
A.一定只有C、H B.可能含有C、H、O
C.一定含有C、H、无O D.一定含有C、H、可能有O
下列有机物不能通过加成反应制取的是
| A.CH3CH2Cl | B.CH2ClCH2Cl | C.CH3CH2OH | D.CH3COOH |
下列有关煤、石油、天然气等资源的说法正确的是
| A.石油裂解得到的汽油是纯净物 | B.石油产品都可用于聚合反应 |
| C.天然气是一种清洁的化石燃料 | D.煤就是碳,属于单质 |
下列气态氢化物中最稳定的是
| A.CH4 | B.SiH4 | C.H2S | D. HCl |
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是
| A.原子半径:A>B>D>C | B.原子序数:d>c>b>a |
| C.离子半径:C3->D->B+>A2+ | D.单质还原性:A>B>D>C |