小美在奥运五连环中填入了5种物质,相连环物质间能发生反应,不相连环物质间不能发生反应。你认为“五连环”中物质间发生的反应,没有涉及的基本反应类型和属于氧化还原反应的个数有
| A.复分解反应、1个 |
| B.分解反应、2个 |
| C.化合反应、3个 |
| D.置换反应、2个 |
能正确表示下列反应的离子方程式是( )
A.用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-=2AlO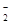 +H2O +H2O |
B.氯化钠与浓硫酸混合加热:H2SO4+2Cl-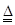 SO2↑+Cl2↑+H2O SO2↑+Cl2↑+H2O |
| C.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+3H2O |
D.硫酸氢钠溶液中滴入Ba(OH)2溶液使所得溶液呈中性:Ba2++OH-+H++SO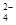 =BaSO4+H2O =BaSO4+H2O |
下列叙述正确的是( )
| A.甘油与丙三醇互为同系物 |
| B.不同元素的原子构成的分子只含极性共价键 |
C.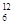 C和 C和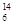 C是中子数不同质子数相同的同种核素 C是中子数不同质子数相同的同种核素 |
| D.短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
化学来源于生活,并应用于生产生活中。下列关于化学与生产、生活的认识不正确的是
| A.将煤气化、液化等方法处理,是提高燃料燃烧效率的重要措施之一 |
| B.CO2、CH4、N2等均是造成温室效应的气体 |
| C.甲醇、天然气、液化石油气、氢气都可以作为燃料电池的原料,其中氢气是最为环保的原料 |
| D.合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 |
常温常压下,乙烷、乙炔和丙烯组成的混合烃64mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了112 mL,原混合烃中乙炔的体积分数为( )
| A.12.5% | B.25% | C.50% | D.75。 |
一定条件下存在反应:2SO2(g)+O2(g) 2SO3(g),△H=-QkJ·mol-1。现有三个体积固定的容器I、II、III,体积分别为1L、1L和2L,其中I、II为绝热容器,III为恒温容器,各容器中充入的物质的量(mol)如下表:
2SO3(g),△H=-QkJ·mol-1。现有三个体积固定的容器I、II、III,体积分别为1L、1L和2L,其中I、II为绝热容器,III为恒温容器,各容器中充入的物质的量(mol)如下表:
| SO2 |
O2 |
2SO3 |
|
| I |
2 |
1 |
0 |
| II |
0 |
0 |
2 |
| III |
2 |
1 |
2 |
下列说法正确的是
A.容器I、II中产生的总热量(只考虑热值,不考虑符号)小于Q
B.容器I、III中反应的平衡常数相同
C.按起始加入的各物质的量将容器I与容器II无缝对接后,达到平衡后,各物质的量浓度与容器III平衡时浓度相同
D.平衡后,SO2的正反应速率大小关系:I>III>II