下列实验中,合理的是
| A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
B.用100mL 量筒量取5.2m L 盐酸 L 盐酸 |
| C.用托盘天平称取25.28g NaCl固体 |
| D.用100mL 容量瓶配制125mL 0.1mol·L-1盐酸 |
与主族元素在元素周期表中所处的位置有关的是
| A.相对原子质量 | B.核内中子数 |
| C.次外层电子数 | D.电子层数和最外层电子数 |
下列化学用语书写正确的是
A.CH4分子的球棍模型: |
B.硫原子的结构示意图: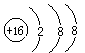 |
C.氮气的电子式: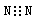 |
D.水分子的结构式: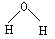 |
下列说法中,错误的是
| A.元素周期表中有7个主族、7个副族 | B.碳元素位于第二周期IVA族 |
| C.稀有气体元素原子的最外层电子数均为8个 | D.氢分子中的化学键是共价键 |
澳大利亚研究人员开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫”,他外形类似海绵,比重极小,并具有磁性。纳米泡沫碳与金刚石的关系是
| A.同素异形体 | B.同分异构体 | C.同一种物质 | D.同位素 |
等质量的两份锌粉a、b分别加入到两份质量相同的过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,下列各图为产生H2的体积V(L)与时间t(min)的关系,其中正确的是()