BaCO3与稀硝酸反应,正确的离子方程式是 ( )
| A.Ba2++ CO32-+2H+=Ba(NO3)2+ H2O+CO2↑ |
| B.BaCO3+2H++2NO3-= Ba(NO3)2+ H2O+CO2↑ |
| C.BaCO3+2H+= Ba2++ H2O+CO2↑ |
| D.CO32-+2H+= H2O+CO2↑ |
如图所示装置,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积比最接近于
| A.2:7 | B.4:5 | C.5:4 | D.7:6 |
离子反应、复分解反应、置换反应和氧化还原反应之间可用集合关系表示,正确的是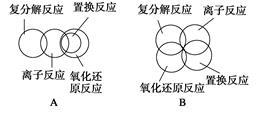
由两种金属组成的混合物12 g,与足量的稀硫酸反应后,在标准状况下产生H2为11.2L,这种金属混合物可能是
| A.Na与Mg | B.Fe与Zn | C.Al与Cu | D.Mg与Zn |
下列各项中,括号里的物质是除杂质所选用的药品,其中错误的是
| A.NaOH中混有Na2CO3(盐酸) |
| B.CO中混有CO2(石灰水) |
| C.H2中混有HCl(NaOH溶液) |
| D.KNO3溶液中混有KCl(AgNO3溶液) |
硫代硫酸钠可作为脱氯剂,已知25.0 mL 0.100 mol·L-1Na2S2O3溶液恰好把224 mL(标准状况下) Cl2完全转化为Cl-,则S2O32—将转化为
| A.S2- | B.SO32- | C.S | D.SO42- |