标准状况下,将V L气体(摩尔质量为M g/mol)溶于0.2L水中,所得溶液的密度是a g/cm3,则此溶液的物质的量浓度(mol/L)为( )
A.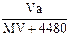 |
B.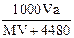 |
C.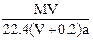 |
D.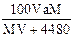 |
“绿色化学”要求从根源上减少或杜绝污染,下列对农作物收割后留下的秸秆的处理方法中,不符合“绿色化学”的是
| A.加工成饲料 | B.发酵后作农家肥 | C.就地焚烧 | D.制造沼气 |
下列拟采用的金属防腐措施,错误的是
| A.给金属衣架或电线外面包上一层塑料层 | B.给自行车钢圈镀上一层金属铬 |
| C.将铁闸门与直流电源正极相连 | D.给铁栅栏表面涂上一层油漆 |
水对人类的生存具有非常重要的意义,没有水就不可能有生机勃勃的地球,所以保护水资源是人类共同的责任。下列各项能造成水质严重污染的是
①生活污水的任意排放 ②海上油轮的原油泄漏 ③水力发电 ④农药化肥的不合理使用 ⑤使用无磷洗衣粉
| A.只有①②③ | B.只有①②④ | C.只有③⑤ | D.只有②③⑤ |
右图照片显示:一只可爱小猫站在一块高分子合成材料上,下面烈火灼烧而小猫却若无其事。这说明此高分子材料一定具有的性质是
| A.良好的绝缘性 | B.良好的绝热性 |
| C.良好导热性 | D.熔点低 |
下列关于药物的使用说法正确的是
| A.因碘酒使蛋白质变性,故常用于外用消毒 |
| B.使用青霉素时,直接静脉注射可以不用进行皮肤敏感试验 |
| C.长期大量使用阿司匹林可预防疾病,没有副作用 |
| D.能用于治疗胃酸过多的抗酸药通常含有麻黄碱 |