铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸的溶液中含有的大量阳离子是 ;X与过量浓硝酸反应后溶液中含有的盐的化学式为 。
(2)某溶液中有Mg2+、Fe2 +、A13+、Cu2+等四种离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐
+、A13+、Cu2+等四种离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐 酸中,所得溶
酸中,所得溶 液与原溶液相比,溶液中大量减少的阳离子是 ;
液与原溶液相比,溶液中大量减少的阳离子是 ;
A.Mg2+ B.Fe2+ C.A13+ D.Cu2+
(3)氧化铁是重要工业颜料,用废秩屑制备它的流程如下: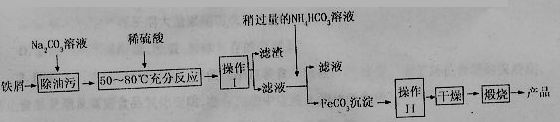
回答下列问题:
①操作I的名称是 ,操作II的名称是 ;操作III的
方法为  。
。
②Na2CO3溶液可以除油污,原因是(用离子方程式表示) ;
③请完成生成FeCO3沉淀的离子方程式 。
(4)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定
(5Fe2++MnO-4+8H+====5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需 。
②该实验中的KMnO4溶液需要酸化,用于酸化的酸是 。
A.稀硝酸 B.稀盐酸 C.稀硫酸 D.浓硝酸
③某同学设计的下列滴定方式,最合理的是 。(夹持部分略去)(填字母序号)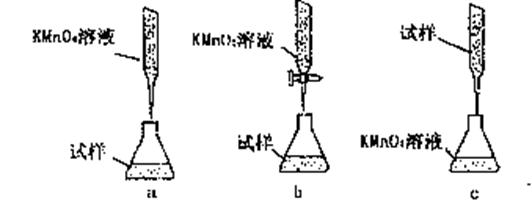
对MgCl2、Al2O3、Fe2O3和SiO2组成的混合物进行下列处理,以制取金属Z,并提纯氧化铝。
(1)①和②步骤中分离溶液和沉淀的操作是:
(2)金属Z名称为;残渣A为,固体C是
(3)滤液B的溶质有(填化学式)
(4)写出电解Y 的化学方程式
(5)写出X→B的离子方程式
(6)实验室里常往AlCl3溶液中加入(填“氨水”或“NaOH溶液”)来制取Al(OH)3固体,其反应的离子方程式为
下表为元素周期表的一部分,根据表中所列出的元素回答下列问题
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
C |
N |
O |
F |
||||
| 3 |
Na |
Mg |
Al |
Si |
S |
Cl |
Ar |
(1)最不活泼的元素是(填元素符号,下同),最活泼的非金属元素是
(2)可做半导体材料的元素是(填元素名称)
(3)氧离子结构示意图为,C、N、O原子半径从大到小的顺序是
(4)与水反应最剧烈的金属单质是,其反应的化学方程式是
(5)既能与强酸又能与强碱反应的金属单质是
(6)最高价氧化物的水化物中酸性最强的酸是(写化学式)
(7)气态氢化物的稳定性:H2SHCl(填“>”、“=”或“<”);
(8)Al2O3中铝元素与氧元素的质量比是,氧元素质量分数为
A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性。下述为相关实验步骤和实验现象: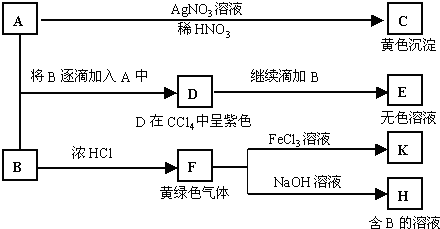
请回答:
(1)写出A和C的化学式:AC 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
_________________________________、___________________________________。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:_____________________________。
(4)写出由F→H的化学方程式:__________________________________________。
某反应体系的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。
(1)请将Au2O3之外的反应物与生成物分别填入以下空格内。
(2)反应中,被还原的元素是_______,还原剂是____________。
(3)将氧化剂与还原剂填入空格中,并标出电子转移的方向和数目。
(4)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂与氧化剂物质的量之比为__________。
有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有全部标出)。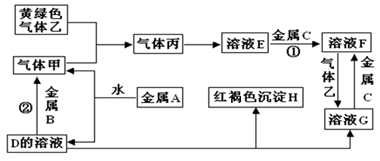
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A______________;H ___________;G________;乙__________;
(2)写出下列反应的化学方程式
反应①____________________________________________。
反应②____________________________________________。