把0.05molBa(OH)2固体分别加入到下列100mL液体中,溶液导电性基本不变。该液体是
| A.自来水 | B.1.0mol/L盐酸 | C.0.5mol/L硫酸 | D.1.0mol/L氨水 |
碱性硼化钒(VB2)—空气电池工作时反应为:4VB2 + 11O2 = 4B2O3 + 2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是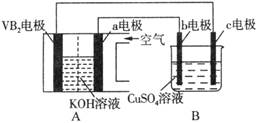
| A.VB2电极发生的电极反应为:2VB2 + 11H2O - 22e- = V2O5 + 2B2O3 + 22H+ |
| B.外电路中电子由c电极流向VB2电极 |
| C.电解过程中,c电极表面先有红色物质析出,后有气泡产生 |
| D.若B装置内的液体体积为100 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L |
下列说法不正确的是
A.某有机物的结构简式如图所示 ,该物质属于芳香族化合物是苯的含氧衍生物,含有两种含氧官能团 ,该物质属于芳香族化合物是苯的含氧衍生物,含有两种含氧官能团 |
| B.按系统命名法,有机物(CH3)2CHCH(CH2CH3)(CH2CH2CH3)的命名为:2-甲基-3-乙基己烷 |
| C.总质量一定时,乙炔和乙醛无论按什么比例混合,完全燃烧消耗氧气量或生成CO2量不变 |
| D.丙烯酸(CH2=CHCOOH)和山梨酸(CH3CH=CHCH=CHCOOH)不是同系物,它们与氢气充分反应后的产物才是同系物。 |
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价的绝对值相等,Z的核电荷数是Y的2倍,W的最外层电子数是最内层电子数的3倍。下列说法不正确的是
| A.化合物YR4中各原子均满足8电子稳定结构 |
| B.对应原子半径:Z<W<R |
| C.W与X、W与Y形成的化合物化学键类型完全相同 |
| D.Y的最高价氧化物对应的水化物是弱酸 |
下列有关实验设计或操作、观察或记录、结论或解释都不正确的是
| 选项 |
实验设计或操作 |
观察或记录 |
结论或解释 |
| A |
将少量浓硝酸分多次加入Cu和稀硫酸的混合液中 |
可看到红棕色气体,后出现无色气体 |
硝酸的还原产物是NO,红棕色是因为NO与空气中的氧气反应所生成的。 |
| B |
某粉末用酒精润湿后,用铂丝蘸取做焰色反应 |
火焰呈黄色 |
该粉末一定不含钾盐 |
| C |
在AlCl3和MgCl2的混合液中加入过量NaOH溶液 |
先生成白色沉淀,后沉淀部分溶解 |
金属性Na>Mg>Al |
| D |
将盛水的分液漏斗先静置,再旋转180度,再倒置 |
漏斗口和活塞不渗水 |
分液漏斗不漏液 |
下列相关化学知识的说法正确的是
| A.利用外接直流电源保护铁质建筑物,属于电化学中牺牲阳极的阴极保护法 |
| B.分类方法、统计方法、定量研究、实验方法和模型化方法等是化学研究的常用方法 |
| C.蛋白质和油脂在一定条件下都能水解,水解产物不同,但两者都属于高分子化合物 |
| D.分子数为NA的C2H4气体体积约为 22.4 L,其质量为 28 g(N A-阿伏加德罗常数) |