已知:(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) △H="74.9" kJ·mol-1,下列说法中正确的是
| A.该反应中熵变、焓变皆大于0 |
| B.该反应是吸热反应,因此一定不能自发进行 |
| C.碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定自发进行 |
| D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 |
对照实验是研究物质性质的一种重要方法,下列不是用来作对照实验的是()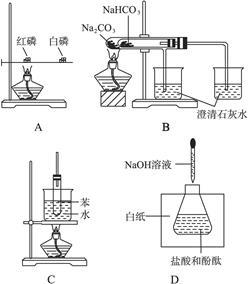
下列装置或操作能达到实验目的的是( )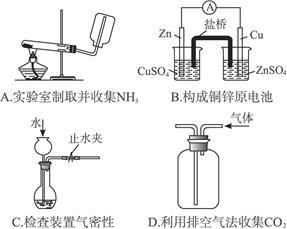
下列有关实验操作错误的是()
| A.用药匙取用粉末状或小颗粒状固体 | B.用胶头滴管滴加少量液体 |
C.给盛有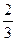 体积液体的试管加热 体积液体的试管加热 |
D.倾倒液体时试剂瓶标签面向手心 |
下列实验操作完全正确的是()
| 编号 |
实验 |
操作 |
| A |
钠与水反应 |
用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| B |
配制一定浓度的氯化钾溶液1 000 mL |
准确称取氯化钾固体,放入到1 000 mL的容量瓶中,加水溶解,振荡摇匀,定容 |
| C |
排除碱式滴定管尖嘴部分的气泡 |
将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 |
| D |
取出分液漏斗中所需的上层液体 |
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
下列实验方法合理的是( )
| A. | 可用水鉴别己烷、四氯化碳、乙醇三种无色液体 |
| B. | 油脂皂化后可用渗析的方法使高级脂肪酸钠和甘油充分分离 |
| C. | 可用澄清石灰水鉴别 溶液和 溶液 |
| D. | 为准确测定盐酸与 溶液反应的中和热,所用酸和碱的物质的量相等 |