.选择萃取剂将碘水中的碘萃取出来,这种萃取剂应具备的性质是( )





 B
B
| A.不溶于水,且必须易与碘发生化学反应 |
B.不溶于水,且碘在其中的溶解度大于水中溶解度 |
| C.不溶于水,且必须比水密度大 |
| D.不溶于水,且必须比水密度小 |
下列实验操作正确的是 ( )。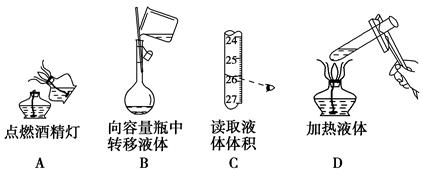
由草木灰提取钾盐并检验含有的钾元素,下列实验操作错误的是 ( )。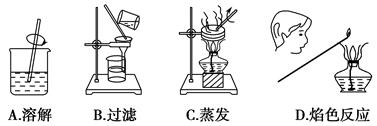
下列实验中指定使用的仪器必须预先干燥的是 ( )。
①中和热测定实验所用的小烧杯
②中和滴定实验所用的锥形瓶
③配制一定物质的量浓度溶液的实验所用的容量瓶
④喷泉实验用于收集NH3的烧瓶
| A.①② | B.①④ | C.②③ | D.③④ |
下列有关技术手段或仪器在化学研究中的应用的说法不正确的是 ( )。
| A.用电子天平可直接称出某个分子或原子的质量 |
| B.用pH计测定溶液的pH |
| C.用移液管量取25.00 mL溶液 |
| D.用量热计测定某些化学反应的反应热 |
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O,则下列说法正确的是 ()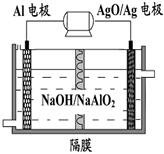
A.该隔膜是阳离子交换膜 |
| B.正极的电极反应式为:O2+2H2O+4e-=4OH- |
| C.负电极的反应式为:Al-3e-= Al3+ +2H2O |
| D.当电极上析出5.4 g Ag时,电路中转移的电子为0.1mol |