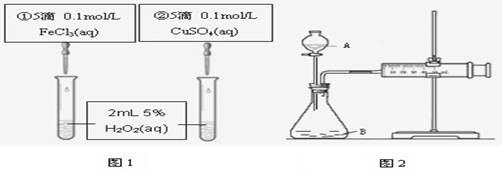
为探究Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两组同学分别设计了如图1、图2所示的实验。下列叙述中不正确的是
| A.图1实验可通过观察产生气泡的快慢来比较反应速率的大小 |
| B.若图1所示的实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好 |
| C.用图2装置比较反应速率,可测定在相同状况下反应产生的气体体积及反应时间 |
| D.为检查图2装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否复原 |
常温下向10 mL 0.1mol·L–1氨水中缓缓加蒸馏水稀释到1 L后,下列变化中正确的是
①电离程度增大;②c(H+)增大;③导电性增强;④ 不变;⑤OH–数目增大,H+数目减小;⑥pH增大;⑦ c(H+)与c(OH–)的乘积减小
不变;⑤OH–数目增大,H+数目减小;⑥pH增大;⑦ c(H+)与c(OH–)的乘积减小
| A.①②④ | B.①⑤⑥ | C.除②外都正确 | D.①④⑤⑥⑦ |
常温下,有关①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液,四种溶液的比较中,正确的是
| A.水电离的c(H+):①=②=③=④ |
| B.将②、③溶液混合后pH=7,则消耗溶液的体积:②=③ |
| C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大 |
| D.向溶液中加入100mL水后,溶液的pH:③>④>①>② |
下列实验误差分析错误的是
| A.用湿润的pH试纸测稀碱液的pH,测定值偏小 |
| B.用容量瓶配置溶液,定容时俯视刻度线,所配溶液浓度偏小 |
| C.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小 |
| D.测定中和反应反的应热时,将碱缓慢倒入酸中,所测温度值偏小 |
合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为CO(g)+ H2O(g) CO2(g) + H2(g)△H<0反应达到平衡后,为提高CO的转化率,下列措施中正确的是
CO2(g) + H2(g)△H<0反应达到平衡后,为提高CO的转化率,下列措施中正确的是
| A.增加压强 | B.降低温度 | C.增大CO 的浓度 | D.更换催化剂 |
下列事实不能用勒夏特列原理解释的是
A.溴水中有下列平衡Br2+H2O HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 |
| B.合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 |
C.反应CO(g)+NO2(g) CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 |
D.对于2HI(g) H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 |