从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。下图表示了三种金属被人类开发利用的大致年限,之所以有先后,主要取决于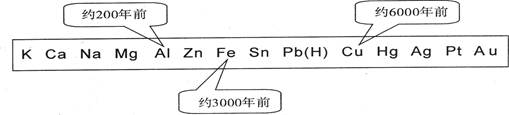
| A.金属的化合价高低 | B.金属的活动性大小 |
| C.金属的导电性强弱 | D.金属在地壳中的含量多少 |
25℃时,下列各组离子在指定溶液中一定能大量共存的是
| A.pH=14的溶液中:K+、Ca2+、HCO3-、SO42- |
B.常温下,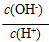 =10﹣10的溶液中:Na+、NH4+、SO42-、NO3- =10﹣10的溶液中:Na+、NH4+、SO42-、NO3- |
| C.c(ClO﹣)=1.0mol·L﹣1的溶液中:Na+、SO32-、S2-、SO42- |
| D.0.1 mol·L﹣1的NaAlO2溶液中:NH4+、Fe3+、Cl﹣、I﹣ |
用下图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是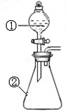
| 选项 |
①中物质 |
②中物质 |
预测②中的现象 |
| A. |
稀盐酸 |
碳酸钠与氢氧化钠的混合溶液 |
立即产生气泡 |
| B. |
浓硝酸 |
用砂纸打磨过的铝条 |
产生红棕色气体 |
| C. |
新制氯水 |
淀粉碘化钾溶液 |
溶液变蓝色 |
| D. |
浓盐酸 |
二氧化锰 |
产生黄绿色气体 |
CuSO4溶液中加入过量KI溶液,产生白色CuI沉淀,溶液变棕色。向反应后溶液中通入过量SO2,溶液变成无色。下列说法不正确的是
| A.滴加KI溶液时,KI被氧化,CuI是还原产物 |
| B.通入SO2后,溶液变无色,体现SO2的还原性 |
| C.上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |
| D.整个过程发生了复分解反应和氧化还原反应 |
已知甲、乙、丙、X是四种中学化学中常见的物质,其转化关系如图所示。则甲和X 不可能是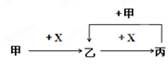
| A.甲为C,X为O2 |
| B.甲为NaOH溶液,X为SO2 |
| C.甲为Fe,X为Cl2 |
| D.甲为AlCl3,X为NaOH溶液 |
设NA为阿伏伽德罗常数的数值,下列说法正确的是
| A.常温常压下,14 g C2H4、C3H6的混合气体中含有碳原子的数目为NA |
| B.常温下,pH=12的Na2CO3溶液中含有的OH-离子数为0.01NA |
| C.标准状况下,0.56 L丙烷中含有共价键的数目为0.2 NA |
| D.含0.2mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA |