考查以下涉及H2O2的反应(未配平):
①Na2O2+HCl H2O2+NaCl
H2O2+NaCl
②Ag2O+H2O2 Ag+O2↑+H2O
Ag+O2↑+H2O
③H2O2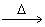 H2O+O2↑
H2O+O2↑
④H2O2+Cr2(SO4)3+KOH K2CrO4+K2SO4+H2O
K2CrO4+K2SO4+H2O
判断下列说法正确的是 ( )
| A.都是氧化还原反应 | B.反应④中还原性:H2O > Cr2(SO4)3 |
| C.发生还原反应的元素相同 | D.H2O2既有氧化性,又有还原性 |
有关能量的判断或表示方法正确的是 ( )
| A.由:H+(aq) + OH-(aq)= H2O(l)△H =-57.3kJ/mol,可知:含1mol CH3COOH的溶液与含1mol NaOH的溶液混合,放出热量等于57.3 kJ |
| B.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
| C.从C(石墨)= C(金刚石)△H =" +" 1.9kJ/mol,可知石墨比金刚石更稳定 |
| D.2gH2完全燃烧生成液态水放出285.8kJ热量,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)="2" H2O(l)△H =-285.8kJ/mol |
全钒液流电池是一种新型的绿色环保储能电池,该电池性能优良,其电池总反应为:V3++VO2++H2O VO2++2H++V2+。下列叙述正确的是 ( )
VO2++2H++V2+。下列叙述正确的是 ( )
| A.充电时阳极附近溶液的酸性减弱 |
| B.充电时阳极反应式为:VO2++2H++e-=VO2++H2O |
| C.放电过程中电解质溶液中阳离子移向负极 |
| D.放电时每转移1mol电子,负极有1mol V2+被氧化 |
用惰性电极电解50 mL锰酸钾溶液:K2MnO4+H2O→KMnO4+H2↑+KOH(未配平),当生成112 mL氢气(标准状况)时停止通电。下列判断正确的是 ()
| A.K+浓度减小 | B.KMnO4在阳极区生成 |
| C.阴极周围溶液的pH减小 | D.反应过程中共转移0.005mol电子 |
某小组为研究电化学原理,设计如图装置。下列叙述不正确的是( )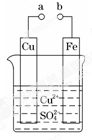
| A.a 和 b 不连接时,铁片上会有金属铜析出 |
| B.a 和 b 用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu |
| C.无论 a 和 b 是否连接,铁片均会溶解,溶液均从蓝色逐渐变 成浅绿色 |
| D.a 和 b 分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 |
将两个铂电极放置在KOH溶液中,然后分别向两极通入CH4和O2,即可产生电流,称为燃料电池,下列叙述正确的是( )
①通入CH4的电极为正极;②正极的电极反应式是O2+2H2O+4e-=4OH-;③通入CH4的电极反应式是CH4+2O2+4e-=CO2+2H2O;④负极的电极反应式是CH4+10OH--8e-=CO32-+7H2O;⑤放电时溶液中的阳离子向负极移动;⑥放电时溶液中的阴离子向负极移动。
| A.①③⑤ | B.②④⑥ | C.④⑤⑥ | D.①②③ |