下列判断正确的是 ( )
| A.元素周期表中查得的相对原子质量为同使素的相对原子质量 |
| B.化学键的变化一定会引起化学反应的变化 |
| C.酸性氧化物一定是非金属氧化物 |
| D.钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水 |
钛(Ti)被称为继铁、铝之后的第三金属,由TiO2制取Ti的主要反应有:
①TiO2+2C+2Cl2TiCl4+2CO
②TiCl4+2Mg2MgCl2+Ti
下列叙述正确的是
| A.反应①是置换反应 | B.TiCl4在反应中做催化剂 |
| C.反应①中TiO2是氧化剂 | D.反应②说明Mg比Ti活泼 |
下图所示装置是化学实验室的常用装置,它有多种用途.以下各项用途和操作都正确的是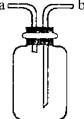
| A.干燥CO2:瓶内放一定体积浓硫酸,由a进气 |
| B.用于收集O2:瓶内充满水,由b进气 |
| C.提供少量CO:瓶内充满CO,b接进水管 |
| D.用做H2S和SO2反应的装置:由a通入H2S,b通入SO2 |
(已知:2H2S+SO2=3S+2H2O)
某溶液中大量存在以下浓度的五种离子:0.2 mol/L Cl-、0.4 mol/L SO42-、0.1 mol/L Al3+、0.3 mol/L H+、M,则M及物质的量浓度可能为
| A.Na+ 0.3 mol/L | B.Zn2+ 0.2 mol/L | C.CO32- 0.2 mol/L | D.Ca2+ 0.1 mol/L |
下列实验操作正确的是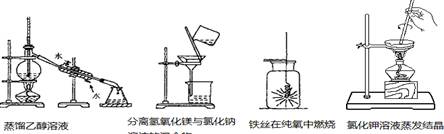
ABC D
在遇铁粉能产生大量气体的溶液中,可以大量共存的是
| A.K+、Cl-、NO、CH3COO- | B.Na+、Ca2+、Cl-、HCO |
| C.Na+、SO42-、NH4+、NO | D.Ba2+、K+、NO、SO42- |