高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程。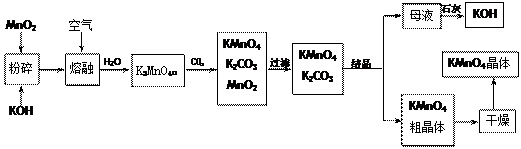
(1)KMnO4稀溶液是一种常用的消毒剂。其消毒机理与下列 (填序号)物质相似。
| A.75%酒精 | B.双氧水 | C.苯酚 |
| D.84消毒液(NaClO溶液) |
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
。
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是: 。
(4)上述流程中可以循环使用的物质有石灰、二氧化碳、 和 写化学式)。
(5)若不考虑物质循环与制备过程中的损失,则1 mol MnO2可制得 mol KMnO4。
某烃化学式为C8H10能使酸性KMnO4溶液褪色,溴水不能褪色,该烃具有_______种同分异构体,其中苯环上的一氯代物只有一种,该烃的名称为__________。
(14分) 分别由C、H、O三种元素组成的有机物A、B、C互为同分异构体,它们分子中C、H、O元素的质量比为15︰2︰8,其中化合物A的质谱图如下。
A是直链结构,其核磁共振氢谱有三组峰,且峰面积之比为1︰1︰2,它能够发生银镜反应。B为五元环酯。C的红外光谱表明其分子中存在甲基。其它物质的转化关系如下:
⑴A的分子式是:。A分子中的官能团名称是:。
⑵B和G的结构简式分别是:、。
⑶写出下列反应方程式(有机物用结构简式表示)
D→C;
H→G。
⑷写出由单体F分别发生加聚反应生成的产物和发生缩聚反应生成的产物的结构简式:、。
(8分)选择适当的试剂除去下列各组括号中的杂质,写出除杂反应的化学方程式,并注明反应类型:
⑴乙烷(乙烯):除杂试剂:,反应方程式:,
反应类型:。
⑵乙酸乙酯(乙酸):除杂试剂:,反应方程式:,
反应类型:。
如下图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略。将封闭有甲烷和氯气的混和气体的装置放置在有光亮的地方,让混和气体缓慢的反应一段时间。
(1)假设甲烷与氯气反应充分,且只产生一种有机物,写出化学方程式:
(2)经过几个小时的反应后,U型管右端的玻璃管中水柱变化是。
A.升高 B.降低 C.不变 D.无法确定
(3)U型管左端的气柱变化是。
A.体积增大 B.体积减小 C.消失 D.不变
(4)试解释U型管右端的玻璃管中水柱变化的原因。
在密闭容器中,通入xmolH2和ymolI2(g),改变下列条件,反应速率将如何改变?(填“增大”、“减小”或“不变”)
(1)升高温度;
(2)加入催化剂;
(3)容器容积充入H2;
(4)扩大容器的体积
(5)容器容积不变,通入氖气