.某溶液中含有 、
、 、
、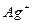 ,现用
,现用 溶液、盐酸和
溶液、盐酸和 溶液将这三种离子逐一沉淀分离,其流程如下图所示。下列说法正确的是( )
溶液将这三种离子逐一沉淀分离,其流程如下图所示。下列说法正确的是( )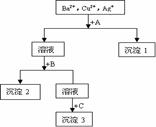
A.试剂A为 溶液 溶液 |
B.沉淀3的化学式可能是 |
C.生成沉淀1的离子方程式为: +2 +2 = =  ↓ ↓ |
D.生成沉淀2的离子方程式为: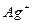 + +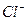 = =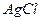 ↓ ↓ |
已知短周期元素的离子aA-、bB2-、cC+、dD2+都具有相同的电子层结构,则下列叙述正确的是
| A.原子半径为D>C>A>B | B.原子序数为a>b>c>d |
| C.离子半径为aA->bB2->cC+>dD2+ | D.a+2=c |
运用元素周期律分析下面的推断,其中错误的是
| A.硒化氢是无色、有毒、比硫化氢稳定的气体 |
| B.砹化银不溶于水也不溶于稀硝酸 |
| C.硫酸镭是难溶于水的白色固体 |
| D.锗单质是一种优良的半导体材料 |
表明金属甲比金属乙活动性强的叙述正确的是
| A.在氧化还原反应中,甲失的电子比乙多 |
| B.将甲和乙用导线相连接,一同放入CuSO4溶液中,乙的表面有红色的铜析出 |
| C.同价态阳离子,甲比乙氧化性强 |
| D.将甲、乙组成原电池时,甲为正极 |
下列变化中既有离子键断裂,又有共价键断裂的是
| A.NaCl溶于水 | B.HCl溶于水 |
| C.干冰气化 | D.KClO3受热分解 |
下列排列顺序不正确的是
| A.热稳定性:HF>HCl>HBr | B.原子半径:Na>S>O |
| C.酸性:H3PO4>H2SO4>HClO4 | D.元素金属性:Na>Mg>Al |