a mol FeS与b mol FeO投入到VLc mol/L稀硝酸中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )
①(a+b)×63g ②(a+b)×189g
③(a+b)mol ④[cV- ]mol
]mol
| A.①④ | B.②④ | C.②③ | D.①③ |
在①金刚石②晶体硅③石英④白磷⑤甲烷等五种物质中,分子结构为正四面体的是
| A.①⑤ | B.①②⑤ | C.①②③⑤ | D.④⑤ |
在100mL某混合溶液中,c(HNO3)=0.4mol/L,c(H2SO4)=0.1mol/L,向其中加入 1.92g铜粉,微热,充分反应后溶液中c(Cu2+)为 ( )
| A.0.15mol/L | B.0.3mol/L | C.0.225mol/L | D.无法计算 |
某有机物与过量的金属钠反应,得到VA升气体,另一份等质量的该有机物与小苏打反应得到气体VB升(同温、同压),若VA>VB(VB≠0),则该有机物可能是()
| A.HOCH2CH2OH | B.CH3COOH | C.HOOC-COOH | D.HOOC-C6H4-OH |
经一定时间后,可逆反应aA+bB  cC中物质的含量A%和C%随温度的变化曲线如右图所示。下列说法正确的是()
cC中物质的含量A%和C%随温度的变化曲线如右图所示。下列说法正确的是()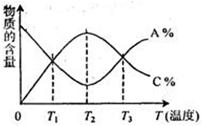
| A.该反应在T1、T3温度时达到化学平衡 |
| B.该反应在T2温度时达到化学平衡 |
| C.该反应的逆反应是放热反应 |
| D.升高温度,平衡会向正反应方向移动 |
mA(g)+nB(g)  pC(g)(正反应为放热反应)的可逆反应,在恒温条件下,平衡时B在混合物中的含量(B%)与压强的关系如图2-32中实线所示,有关叙述正确的是()
pC(g)(正反应为放热反应)的可逆反应,在恒温条件下,平衡时B在混合物中的含量(B%)与压强的关系如图2-32中实线所示,有关叙述正确的是()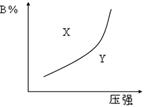
| A.m+n> p |
| B.x点的速率关系为v正>v逆 |
| C.n>p |
| D.x点比y点混合物反应速率快 |