下列说法正确的是( )
①pH=2和pH=1的HNO3中c(H+)之比为1∶10
②0.2 mol·L-1与0.1 mol·L-1醋酸中,c(H+)之比大于2∶1
③Na2CO3溶液中c(Na+)与c(CO32-)之比为2∶1
④纯水在100 ℃和20 ℃时,pH前者大
⑤同温时,pH=10的KOH溶液和pH=10的KCN溶液中由水电离的OH-浓度后者大
⑥100 mL 0.1 mol·L-1的醋酸与10 mL 1.0 mol·L-1的醋酸中H+的数目,前者多
| A.①④⑤ | B.①⑤⑥ | C.①②⑤ | D.①②③⑥ |
在t ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g/mL,质量分数为ω,其中含有NH4+的物质的量是b mol,下列叙述正确的是
A.溶质的质量分数ω= ×100% ×100% |
B.溶质的物质的量浓度c=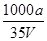 mo/L mo/L |
C.溶液中c(OH-)= mol/L+c(H+) mol/L+c(H+) |
| D.向上述溶液中加入V mL水,所得溶液的质量分数大于0.5ω |
配制0.1 mol/L的NaCl溶液,下列操作会导致所配溶液浓度偏高的是
| A.称量时,左盘高,右盘低 | B.定容时俯视读取刻度 |
| C.容量瓶洗净后未干燥 | D.定容时液面超过了刻度线 |
下列实验操作中,错误的是
| A.配制5%食盐溶液时,将称量的食盐放入烧杯中加适量的水搅拌溶解 |
| B.硫酸铜结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅 |
| C.测定未知NaOH溶液浓度时,酸式滴定管需用标准酸液润洗2~3次 |
| D.配制0.1 mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释 |
有硫酸镁溶液500ml,它的密度为1.20g/cm3,其中镁离子的质量分数为4.8%,则有关该溶液的说法不正确的是
| A.溶质的质量分数为24.0% |
| B.溶液的物质的量浓度为2.4mol/L |
| C.溶质和溶剂的物质的量之比为1:40 |
| D.硫酸根离子的质量分数为19.2% |
由CO、H2和O2组成的混合气体60 mL,在一定条件下恰好完全反应,测得生成物在101 kPa、120℃下对空气的相对密度为1.293,则原混合气体中H2所占的体积分数为
A.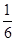 |
B. |
C.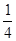 |
D. |