下列说法正确的是
| A.若弱酸HA的电离常数大于弱酸HB的电离常数,则同浓度钠盐溶液的碱性:NaA<NaB |
B.用广泛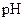 试纸测得0.10mol·L 试纸测得0.10mol·L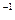 NH4Cl溶液的 NH4Cl溶液的 |
| C.HCl是强电解质,CH3COOH是弱电解质,所以盐酸溶液的导电性强于醋酸溶液 |
| D.将碳酸钾溶液蒸干,得到的固体物质是氢氧化钾 |
下列应用或事实与胶体的性质没有关系的是
| A.用明矾净化饮用水 |
| B.用石膏或盐卤点制豆腐 |
| C.在FeCl3溶液中滴加NaOH溶液出现红褐色沉淀 |
| D.清晨的阳光穿过茂密的林木枝叶所产生的美丽的光线 |
下列物质中属于电解质的是
| A.氢氧化钠固体 | B.二氧化碳气体 | C.铜丝 | D.氨水 |
对下列物质分类全部正确的是
①纯碱 ②食盐水 ③石灰水 ④NaOH ⑤液态氧 ⑥KClO3
| A.碱:①④ | B.纯净物:③④⑤ |
| C.盐:①⑥ | D.混合物:②⑤ |
下列溶液中的Cl-浓度与50 mL 1 mol·L﹣1 MgCl2溶液中的Cl-浓度相等的是
| A.150 mL 1 mol·L-1 NaCl溶液 | B.75 mL 2 mol·L-1 CaCl2溶液 |
| C.150 mL 2 mol·L-1 KCl溶液 | D.75 mL 1 mol·L-1 AlCl3溶液 |
下列反应是氧化还原且不是四种基本反应类型的是
| A.2KMnO4△K2MnO4 + MnO2 + O2↑ |
| B.NaOH + HCl =" NaCl" + H2O |
| C.Fe + CuSO4 =" Cu" + FeSO4 |
| D.Fe2O3 + 3CO 高温 2Fe + 3CO2 |