下列说法正确的是( )
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(g);ΔH=-801.3KJ/mol 结论:CH4的燃烧热为801.3KJ |
B.Sn(s,灰)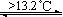 Sn(s,白);ΔH=+2.1KJ/mol(灰锡为粉末状) Sn(s,白);ΔH=+2.1KJ/mol(灰锡为粉末状)结论:锡制品在寒冷的冬天因易转化为灰锡而损坏 |
| C.稀溶液中有:H+(aq)+OH-(aq)=H2O(l);ΔH=-57.3KJ/mol 结论:将盐酸与氨水的稀溶液混合后,若生成1molH2O,则会放出57.3KJ的能量 |
| D.C(s,石墨)+O2(g)=CO2(g);ΔH=-393.5kJ·mol-1, |
C(s,金刚石)+O2(g)=CO2(g);ΔH=-395kJ·mol-1
结论:相同条件下金刚石性质比石墨稳定
下列操作中,能使电离平衡H2O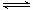 H++OH-,向右移动且溶液呈酸性的是()
H++OH-,向右移动且溶液呈酸性的是()
| A.向水中加入NaHSO4溶液 | B.向水中加入Al2(SO4)3固体 |
| C.向水中加入Na2CO3溶液 | D.将水加 热到100℃,使pH=6 热到100℃,使pH=6 |
现有常温时pH=1的某强酸溶液10mL,下列操作能使溶液的pH变成2的是()
A. 加入10mL 0.01mol·L-1的NaOH溶液 加入10mL 0.01mol·L-1的NaOH溶液 |
B.加入10mL 的水进行稀释 |
| C.加水稀释成100mL | D.加入10mL 0.01mol·L-1的盐酸溶液 |
下列说法正确的是()
| A.pH=2与pH=1的硝酸中c(H+)之比为1:10 |
B.Na2CO3溶液中c(Na+)与c(CO32- )之比为2:1 )之比为2:1 |
| C.0.2 mol•L-1与0.1mol/L醋酸中c (H+)之比为2:1 |
| D.NO2溶于水时,被氧化的n(NO2)与被还原的n(NO2)之比为3:1 |
在2L密闭容器中加入4molA和6molB,发生以下反应:4A(g)+6B(g)  4C(g) +5D(g)。若经5s后,剩下的A是2.5mol,则B的反应速率是()
4C(g) +5D(g)。若经5s后,剩下的A是2.5mol,则B的反应速率是()
| A.0.45 mol / (L·s) | B.0.225 mol / (L·s) | C.0.15 mol / (L·s) | D.0.9 mol / (L·s) |
证明氨水是弱碱的事实是()
| A.氨水与硫酸发生中和反应 |
| B.氨水能使紫色石蕊液变蓝 |
| C.0.1 mol/L的NH4Cl溶液的pH值为5.1 |
| D.铵盐与熟石灰反应逸出氨气 |