下列事实,不能用勒夏特列原理解释的是
| A.实验室用排饱和食盐水而不用排水法收集氯气 |
| B.加催化剂,使N2和H2在一定条件下转化为NH3 |
| C.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施 |
| D.光照新制的氯水时,溶液中c(H+)增大 |
已知键能N≡N 946 kJ/mol ,H-H 436kJ/mol ,N-H 391 kJ/mol.从理论上计算2NH3(g)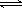 N2(g)+3H2(g)的⊿H为
N2(g)+3H2(g)的⊿H为
| A.-46 kJ/mol | B.-92 kJ/mol |
| C.+92 kJ/mol | D.+1800kJ/mol |
用CH4催化还原NOx可以消除氮氧化合物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ/mol
下列说法中错误的是
| A.等物质的量的CH4在反应①、②中转移电子数相同 |
| B.由反应①可推知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) △H>-574kJ/mol |
| C.4NO2(g)+2N2(g)=8NO(g) △H=+586kJ/mol |
| D.若用标准状况下4.48L CH4把NO2还原为N2,整个过程中转移的电子总数为1.6NA |
下列有关热化学方程式的叙述正确的是
| A.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq) + CH3COOH(aq) = CH3COONa(aq) + H2O(l) △H = -57.4kJ·mol-1 |
| B.已知C(石墨,s)= C(金刚石,s) △H>0,则石墨比金刚石稳定 |
| C.已知反应2H2(g) + O2(g) = 2H2O(l) △H=-571.6kJ·mol-1,则H2的燃烧热为571.6kJ·mol-1 |
| D.已知2C(s)+2O2(g)=2CO2(g) △H1;2C(s)+O2(g)=2CO(g) △H2,则△H1>△H2 |
已知常温下,N2(气)和H2(气)生成2mol NH3(气)放出92.4 kJ热量。现有甲、乙两个容积相同的密闭容器,在常温下:①向密闭容器甲中通入1 molN2和3 mol H2,达到平衡时放出热量Q1kJ。②向密闭容器乙中通入0.5 mol N2和1.5 mol H2,达到平衡时放出热量Q2kJ。则下列关系式正确的是
| A.Q1=2Q2=92.4 | B.Ql>2Q2 | C.Q1<2Q2 | D.Q1=2Q2≠92.4 |
已知:2H2(g)+O2(g)=2H2O(g) △H=-483.6KJ/mol。有关键能数据如下表:
| 化学键 |
H—H |
O=O |
| 键能/KJ▪mol-1 |
436 |
498 |
则水分子中O—H键键能为
A.463.4KJ/mol B.926.8KJ/mol
C.221.6KJ/molD.413KJ/mol