设NA为阿伏加德罗常数,下列说法正确的是:
| A.标准状况下,5.6L四氯化碳含有的分子数为0.25NA |
| B.标准状况下,22.4LCH4中含有的分子总数为5NA |
| C.常温常压下,14g氮气含有的原子数为NA |
| D.标准状况下,铝跟盐酸溶液反应生成1mol氢气时,转移的电子数为NA |
如图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是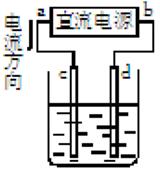
| A.a为负极,b为正极 | B.a为阳极,b为阴极 |
| C.电解过程中,d电极质量增加 | D.电解过程中,氯离子浓度不变 |
某烷烃分子中有124个氢原子,则该烃所含的碳原子数目为
| A.60 | B.61 | C.62 | D.63 |
由乙烯推测丙烯(CH3CH=CH2)的结构或性质正确的是
| A.分子中3个碳原子在同一直线上 | B.分子中所有原子在同一平面上 |
| C.与氯化氢加成只生成一种产物 | D.能发生加聚反应 |
对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
| A.达到化学平衡时,4v正(O2)=5v逆(NO) |
| B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
| C.达到化学平衡时,v正(NH3)=v正(NO) |
| D.化学反应速率关系是3v正(NH3)=2v正(H2O) |
近年来,科学家一直在探索利用铝粉作燃料的可能性,以期望铝能成为一种石油的取代物。假如铝作为一种普遍使用的新型能源被开发利用,下列关于其有利因素的说法中,你认为哪项是错误的
| A.铝质轻,便于运输、贮存且安全 |
B.铝燃烧时放出的热量大,且燃烧 后新产物对环境的污染容易得到有效的控制 后新产物对环境的污染容易得到有效的控制 |
| C.在地球上,铝矿资源丰富 |
| D.现代电冶铝的工业技术已为铝作为新能源奠定了重要基础 |