向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-l Ba(OH)2溶液。随着Ba(OH)2溶液体积(V)的变化,沉淀总物质的量(n)的变化如下图所示。下列说法正确的是 ( )
| A.a点的沉淀总物质的量为0.025mol |
| B.oa段发生反应的离子方程式是: Al3++2SO42-+2Ba2++3OH-=Al(OH)3↓+2BaSO4↓ |
| C.ab段发生反应的离子方程式是: NH4++SO42-+Ba2++OH-=NH3·H2O+BaSO4↓ |
| D.反应至c点,加入Ba(OH)2溶液的总体积为250 mL |
已知:A、B两元素的阴离子具有相同的电子层结构;A元素的阴离子半径大于B元素的阴离子半径;C和B两元素的原子核外电子层数相同;C元素的原子半径大于A元素的原子半径。A、B、C三种元素的原子序数的关系是()
A. B.
B. C.
C.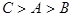 D.
D.
.下列化学用语的书写,正确的是( )
A.氮气的电子式: |
B.硫原子的结构示意图: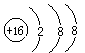 |
C.溴化钠的电子式: |
D.水分子的结构式: |
下列物质的溶液能导电,但不属于电解质的是()
| A.Ba(OH)2 | B.CH4 | C.Cl2 | D.NaCl |
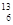 C-NMR(核磁共振)可以用于含碳化合物的结构分析有关
C-NMR(核磁共振)可以用于含碳化合物的结构分析有关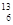 C的说法正确的是
C的说法正确的是
| A.质子数为6 | B.电子数为13 | C.中子数为6 | D.质量数为6 |
Cl与Cl-两种粒子中,相同的是()
| A.化学性质 | B.核外电子数 | C.最外层电子数 | D.核外电子层数 |