某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(已知硝酸只被还原为NO气体)。下列分析或结果不正确的是 ( )
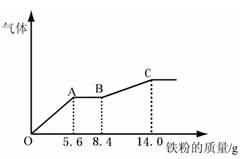
| A.原混合酸中NO3-物质的量为0.2 mol |
| B.原混合酸中H2SO4浓度为2 mol·L-1 |
| C.OA段产生的气体是NO,AB段的反应为Fe+2Fe3+=3Fe2+, BC段产生的气体是氢气 |
| D.第二份溶液中最终溶质为FeSO4 |
已知:4NH (g)+5O
(g)+5O (g)
(g) 4NO(g)+6H
4NO(g)+6H O(g),若反应速率分别用v(NH
O(g),若反应速率分别用v(NH )、v(O
)、v(O )、v(NO)、V(H
)、v(NO)、V(H O)[mol/(L·min)]表示,则下列关系正确的是
O)[mol/(L·min)]表示,则下列关系正确的是
A.4v(NH )=5v(O )=5v(O ) ) |
B.5v(O )=6v(H )=6v(H O) O) |
C.2v(NH )=3v(H )=3v(H O) O) |
D.4v(O )=5v(NO) )=5v(NO) |
从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是
下列与金属腐蚀有关的说法正确的是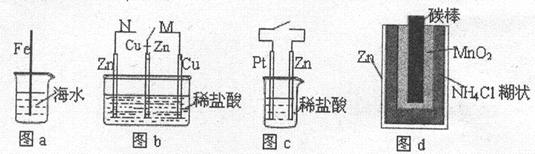
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
D.图d中,工作时NH  的移动方向为由里向外 的移动方向为由里向外 |
元素在周围表中的位置,反映元素的原子结构和元素的性质,下列说法正确的是
| A.同一元素不可能既表现金属性,又表现非金属性 |
| B.第三周期元素的最高正化合价等于它所处的主族序数 |
| C.短周期元素形成离子后,最外层都达到8电子稳定结构 |
| D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
下列实验基本操作正确的是
| A.用pH试纸测得氯水的pH为2 |
| B.做焰色反应需要的仪器有酒精灯与镊子 |
| C.要使稀盐酸的浓度变大可以加热蒸发水分 |
| D.用稀硝酸清洗做过银镜反应实验的试管 |