分类是学习和研究化学的一种常用的科学方法。下列分类合理的是 ( )
①根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等
②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质
④根据元素原子最外层电子数的多少将元素分为金属和非金属
⑤根据反应的热效应将化学反应分为放热反应和吸热反应
⑥根据分散剂的直径大小,分散系可分为溶液、胶体和浊液
| A.②⑤ | B.②③⑥ | C.①②④ | D.②③④⑤ |
8.在2NO2(红棕色)  N2O4(无色)的可逆反应中,下列状态一定达到化学平衡状态的是
N2O4(无色)的可逆反应中,下列状态一定达到化学平衡状态的是
| A.N2O4和NO2的分子数比为1︰2 |
| B.N2O4和NO2的浓度相等 |
| C.单位时间内1 mol N2O4消耗的同时有2 mol NO2生成 |
| D.平衡体系的颜色不再改变 |
7.下列事实中,与电化学腐蚀无关的是
| A.埋在潮湿土壤里的铁管比埋在干燥土壤里的铁管更易被腐蚀 |
| B.为保护海轮的船壳,常在船壳上镶入锌块 |
| C.在空气中,金属银的表面生成一层黑色物质 |
| D.镀银铁制品,镀层部分受损后,露出的铁表面易被腐蚀 |
6.某化学反应的能量变化如下图所示。下列有关叙述正确的是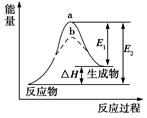
| A.该反应为放热反应 |
| B.E2可表示形成新的化学键所释放的能量 |
| C.该反应的反应热ΔH=E1-E2 |
| D.加入催化剂可同等程度的降低E1、E2 |
5.某温度下,满足下列条件的溶液肯定呈酸性的是
| A.加酚酞显无色的溶液 |
| B.含有H+的溶液 |
| C.pH<7的溶液 |
| D.CH3COOH和NH3·H2O混合液,当c(CH3COO-)> c(NH4+)时 |
4.常温下在水中加入下列物质,不会破坏水的电离平衡的是
| A.通入HCl气体 | B.加入氨水 | C.加入乙醇 | D.加入金属钠 |