25℃、101kPa下,反应2N2O5(g)=4NO2(g)+O2(g) △H=+56.7kJ/mol能自发进行的原因是)
| A.是吸热反应 | B.是放热反应 |
| C.是熵减小的反应 | D.熵增效应大于热效应 |
已知下列热化学方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-24.8kJ·mol-1
②Fe2O3(s)+ CO(g)=
CO(g)=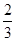 Fe3O4(s)+
Fe3O4(s)+ CO2(g)ΔH=-15.73kJ·mol-1
CO2(g)ΔH=-15.73kJ·mol-1
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH=+640.4kJ·mol-1
则14 g CO气体还原足量FeO固体得到Fe固体和CO2气体时对应的ΔH约为( )
| A.-218kJ·mol-1 | B.-109kJ·mol-1 |
| C.+218kJ·mol-1 | D.+109kJ·mol-1 |
如下图各烧杯中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )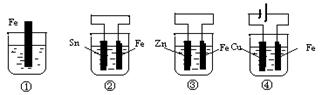
| A.④>②>①>③ | B.②>①>③>④ |
| C.④>②>③>① | D.③>②>④>① |
25℃时,水中存在电离平衡:H2O  H++OH- △H>0。下列叙述正确的是()
H++OH- △H>0。下列叙述正确的是()
| A.将水加热,KW增大,pH不变 |
| B.向水中加入少量NaHSO4固体,c(H+)增大,KW不变 |
| C.向水中加入少量NaOH固体,平衡逆向移动,c(OH-)降低 |
| D.向水中加入少量NH4Cl固体,平衡正向移动,c(OH-)增大 |
下列有关离子大量共存的说法正确的是()
| A.H+、Fe2+、SO42﹣、NO﹣3因发生氧化还原反应而不能大量共存 |
| B.澄清透明的无色溶液中,ClO﹣、MnO4﹣、Al3+、SO2﹣4可能大量共存 |
| C.在含大量Fe3+的溶液中,NH+4、Na+、Cl﹣、SCN﹣可能大量共存 |
| D.使石蕊试液变红的溶液中,Na+、Cl﹣、SO2﹣4、HCO3﹣可以大量共存 |
下列说法不正确的是()
| A.化学反应过程中,一定有化学键的断裂和形成 |
| B.盖斯定律实质上是能量守恒定律的体现 |
| C.反应前后原子种类和数目不变遵循的是质量守恒定律 |
| D.如果某化学反应的DH和DS均小于0,则反应一定能自发进行 |