(1)用18mol·L-1的硫酸配制1.00 mol·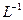 的硫酸100mL。若实验仪器有:
的硫酸100mL。若实验仪器有:
A.100mL量筒、B.托盘天平、C.玻璃棒、D.50mL容器瓶、E. 10mL量筒、
F.胶头滴管、G. 50mL烧杯、H. 100mL容量瓶。
实验时应选用仪器是 (填 字母);
字母);
(2)在容量瓶的使用方法 中,下列操作不正确的是 (填字母);
中,下列操作不正确的是 (填字母);
A.使 用容量瓶前检查其是否漏水。
用容量瓶前检查其是否漏水。
B.容量瓶用蒸馏水洗净后,再用待配溶液洗涤。
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1—2cm处,用胶头滴管滴加蒸馏水到刻度线。
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1—2cm处,用胶头滴管滴加蒸馏水到刻度线。
E.盖好瓶盖,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次
(3)浓H2SO4稀释时应该
;
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响?(填“偏高”、“偏低”或“不变”)
①稀释硫酸后的烧杯未洗涤: ;
②未经冷却趁热将溶液注入容量瓶中: ;
③摇匀后发现液面低于刻度线再加水: ;
④容量瓶中原有少量蒸馏水: 。
已知下列反应的反应热为
①CH3COOH(l)+2O2(g) = 2CO2(g)+2H2O(l)ΔH1=-870.3 kJ/mol
②H2(g)+ O2(g) = H2O(l)ΔH2=-285.8 kJ/mol
O2(g) = H2O(l)ΔH2=-285.8 kJ/mol
(1)已知1.2 g固体C充分燃烧生成CO2放出热量为39.35 kJ,请写出C的燃烧热化学方程式(碳的燃烧热用ΔH3表示):;
(2)计算反应:2C(s)+2H2(g)+O2(g) = CH3COOH(l)的反应热ΔH。(要有计算过程)
某温度下,将4.0 mol的HI气体充入1 L已经抽空的固定容积的密闭容器中,发生如下反应:2HI(g) H2(g)+I2(g) ΔH>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
H2(g)+I2(g) ΔH>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间/s n /mol |
0 |
40 |
80 |
120 |
| n(HI) |
4.0 |
2.8 |
b |
c |
| n(H2) |
0 |
a |
1.0 |
1.0 |
(1)a =,c =;
(2)计算在该温度时此反应的平衡常数K =;
(3)保持温度不变,120 s时再通入2.0 mol的H2。当再次达到平衡时,HI的平衡转化率是多少?(本小题要有适当的解题过程)
Q、R、X、Y、Z五种元素的原子序数依次递增。已知:① Z的原子序数为29,而Q、R、X、Y均为短周期主族元素;② R原子有3个未成对电子;③ Q、X原子p轨道的电子数分别为2和4;④ Y原子价电子(外围电子)排布为msnmpn。请回答下列问题:
(1)R的氢化物RH3中R采取______杂化,其键角_____109°28′(选填“>”、“=”或者“<”)。
(2)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是(选填字母代号)_____。
a.稳定性:甲>乙;沸点:甲>乙
b.稳定性:甲>乙;沸点:甲<乙
c.稳定性:甲<乙;沸点:甲<乙
d.稳定性:甲<乙;沸点:甲>乙
(3)下列与H2X分子互为等电子体的微粒有(选填字母代号)。
a.CH4b.H2Sc.NO2d.NH2-
(4)由X和Y形成的化合物属于________晶体(填晶体类型),30 g该晶体中有_____mol共价键。
(5)Z是(填元素符号),它位于周期表的区,其晶体的三维堆积模型见下图,
称之为面心立方最密堆积,其配位数为。Z2+的外围电子排布式是____________。1个Z2+与4个RH3以配位键结合形成_________________离子(填化学式)。
恒容体系,发生如下反应2A(g) B(g)+xC(g) ΔH,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如图。某课外活动小组一共进行了如图所示的三个实验(其中T1、T2表示不同的反应温度)。
B(g)+xC(g) ΔH,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如图。某课外活动小组一共进行了如图所示的三个实验(其中T1、T2表示不同的反应温度)。
(1)在实验Ⅲ中,0~20min的时间内,v(A)=。
(2)分析实验I和实验II的数据,可知x=;分析实验II和实验Ⅲ的数据,可知反应热ΔH0(选填“>”、“=”或者“<”)。
(3)能说明该反应达到平衡状态的是(选填代号字母)。
a.A的质量不再变化
b.混合气体的密度保持不变
c.用A、B、C表示的反应速率的比为2∶1∶x
d.单位时间内生成n mol B的同时生成2n mol A
e.混合气体的平均摩尔质量保持不变
(4)T1℃时,保持容器的体积不变,若充入a mol A、b mol B、c mol C,达到平衡时C的体积分数为0.4,则a、b、c应满足什么条件。
(1)石墨是层状结构,如下图所示。每一层内的碳原子间通过sp2杂化形成(填代号字母,后同);层与层间存在;石墨的每一个碳原子经过sp2杂化后,还剩下1个未成对电子,在电场作用下能够作定向移动,因而石墨还具有导电性,所以还存在。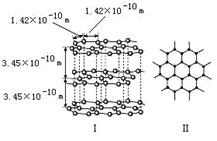
a:σ键
b:π键
c:氢键
d:配位键
e:范德华力
f:金属键
g:离子键
(2)请选“>”、“<”或“=”填与下列空格中:
①熔点:NaMg;②硬度:金刚石晶体硅; ③晶格能:NaINaBr