下列现象或反应的原理解释正确的是
| |
现象或反应 |
原理解释 |
| A |
铝箔在酒精灯火焰上加热熔化但不滴落 |
铝箔表面生成的氧化物具有高熔点 |
| B |
钠和氧气在加热条件下进行反应 |
该反应为吸热反应 |
| C |
碳酸钠和氢氧化钠溶液中滴加酚酞,溶液都呈红色 |
碳酸钠和氢氧化钠都是碱 |
| D |
铁制容器可用于盛装冷的浓硫酸 |
铁与浓硫酸不反应 |
铁片放入下列溶液中,反应时无气体放出,取出后铁片质量减轻,则该溶液是( )
| A.稀硫酸 | B.浓盐酸 | C.AgNO3 | D.Fe2(SO4)3 |
下列反应,其产物颜色按红色、红褐色、淡黄色、蓝色顺序排列的是( )
①金属钠在纯氧中燃烧 ②FeSO4溶液中滴入NaOH溶液并在空气中放置一段时间 ③FeCl3溶液中滴入KSCN溶液 ④无水硫酸铜放入医用酒精中
| A.②③①④ | B.③②①④ | C.③①②④ | D.①②③④ |
将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是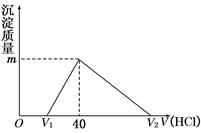
| A.原合金质量为0.92 g | B.标准状况下产生氢气896 mL |
| C.图中V2为60 mL | D.图中m值为1.56 g |
Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2,NO和H2O。当产物n(NO2):n(NO)=1:1时,下列说法正确的是
| A.1 mol Cu2S参加反应时有8 mol电子转移 |
| B.参加反应的n(Cu2S):n(HNO3)=1:5 |
| C.反应中Cu2S既作氧化剂,又作还原剂 |
| D.产物n[Cu(NO3)2] : n[CuSO4 ]=l:1 |
以下示意图与相对应的反应情况分析正确的是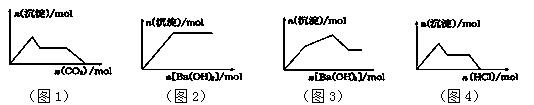
| A.图1 :向含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2 |
| B.图2 :向NaHSO4溶液中逐滴加入Ba(OH)2溶液 |
| C.图3 :向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 |
| D.图4 :向NaAlO2溶液中逐滴加入盐酸 |