通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下列是一些化学键的键能。
| 化学键 |
C—H |
C—F |
H—F |
F—F |
| 键能/(kJ·mol-1) |
414 |
489 |
565 |
155 |
根据键能数据估算下列反应CH4(g)+4F2(g)===CF4(g)+4HF(g)的反应热ΔH为( )
| A.-1940kJ·mol-1 | B.1940kJ·mol-1 |
| C.-485kJ·mol-1 | D.485kJ·mol-1 |
现有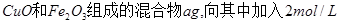 的硫酸溶液50ml,恰好完全反应,若将2
的硫酸溶液50ml,恰好完全反应,若将2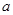 g该混合物在足量
g该混合物在足量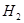 中加热,使其充分反应,冷却后剩余固体质量为()
中加热,使其充分反应,冷却后剩余固体质量为()
A.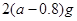 |
B.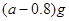 |
C. |
D.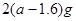 |
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如下图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为 ()
| A.6:1 | B.1:1 | C.2:1 | D.1:2 |
硫代硫酸钠可用做脱氯剂,已知25.0 mL 0.10 mol·L-1Na2S2O3溶液恰好把标准状况下112 mL Cl2完全转化为Cl-,则S2O32-将转化成( )
| A.S2- | B.S | C.SO42- | D. SO32- |
设NA代表阿伏加德罗常数,下列说法正确的是()
| A.标准状况下,22.4 L氦气和1 mol氟气所含原子数均为2 NA |
| B.1 mol Na2O2与CO2反应电子转移为2 NA |
| C.1 mol H2O、1 mol NH3和1mo l OH-所含电子数均为10 NA |
| D.标准状况下22.4L的氯气和某些物质反应,电子转移一定为2 NA |
下列物品或设备:①水泥路桥 ②门窗玻璃 ③水晶项链④石英钟表 ⑤玛瑙手镯 ⑥硅太阳能电池 ⑦光导纤维⑧计算机芯片。所用材料为SiO2或要用到SiO2的是()
| A.①②③④⑤⑦ | B.全部 | C.③④⑤⑦⑧ | D.①②⑦⑧ |