“神舟七号”所用动力燃料之一为氢化锂三兄弟:氕化锂、氘化锂、氚化锂。其中Li的核内中子数为4,有关下列叙述中正确的是( )
| A.三种物质质子数之比为1∶2∶3 |
| B.三种物质中子数之比为1∶1∶1 |
| C.三种物质的摩尔质量之比为8∶9∶10 |
| D.三种物质的化学性质不相同 |
用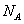 表示阿伏加德罗常数的值。下列判断错误的是()
表示阿伏加德罗常数的值。下列判断错误的是()
A.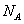 个 个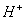 的质量为1 g 的质量为1 g |
B.2 L 0.5mol/L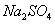 溶液中含 溶液中含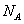 个 个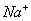 |
C.32 g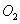 中含有 中含有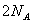 个氧原子 个氧原子 |
D.标准状况下,1 mol 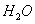 中含有 中含有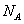 个水分子 个水分子 |
某气体通入品红溶液中,溶液褪色,加热后又恢复为原来颜色,该气体是()
A. |
B. |
C. |
D.Cl2 |
下列有关氢氧化亚铁及其制备方法的叙述中,不正确的是()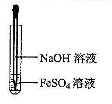
| A.氢氧化亚铁易被空气氧化 |
| B.氢氧化亚铁为灰绿色絮状沉淀 |
| C.可利用右图所示装置,制备氢氧化亚铁 |
| D.实验中所用氢氧化钠溶液应预先煮沸 |
在实验室不能用玻璃试剂瓶盛放的试剂是
| A.氢氟酸 | B.饱和碳酸钠溶液 | C.浓硫酸 | D.氢氧化钠溶液 |
在抗震救灾中要用大量漂白粉和漂白液杀菌消毒,下列说法中正确的是()
| A.漂白粉是纯净物,漂白液是混合物 |
B.漂白粉的有效成分是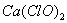 |
| C.工业上将氯气通入澄清石灰水制取漂白粉 |
D.漂白液的有效成分是 |