燃料电池是燃料(如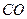 、
、 、
、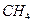 )等跟
)等跟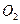 (或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如
(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如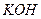 )溶液,下列关于甲烷燃料电池的说法中不正确的是:
)溶液,下列关于甲烷燃料电池的说法中不正确的是:
A.负极的电极反应式为: |
| B.通入氧气的一极发生氧化反应,通入甲烷的一极发生还原反应 |
| C.随着反应的进行,电解质溶液的pH保持不变 |
| D.甲烷燃料电池的能量利用率比甲烷燃烧的大 |
下列药物属于天然药物的是
| A.阿司匹林 | B.青霉素 | C.抗酸药 | D.麻黄碱 |
1997年,第一只“克隆羊”在英国诞生,“克隆羊”的关键技术之一是找到一些特殊的酶,它们能激活普通体细胞,使之像生殖细胞一样发育成个体。下列有关酶的叙述错误的是
| A.酶是具有催化功能的蛋白质 |
| B.酶的催化作用具有选择性和专一性 |
| C.酶通常在强酸或强碱条件下发挥作用 |
| D.高温或紫外线照射会降低酶的活性 |
下列说法正确的是
| A.羧酸和甘油反应生成的酯就是油脂 |
| B.淀粉和纤维素都是纯净物 |
| C.天然油脂都是混甘油酯 |
| D.所有蛋白质遇浓硝酸都会发生颜色反应 |
现在,我们把无污染、无公害的食品叫做绿色食品。而最初,专家把绿色植物通过光合作用转化的食品叫做绿色食品,海洋提供的食品叫做蓝色食品,通过微生物发酵制得的食品叫做白色食品。根据最初的说法,下列属于绿色食品的是
| A.大米 | B.海带 | C.食醋 | D.食盐 |
下列有关蛋白质的叙述中,不正确的是
| A.蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,再加水也不溶解 |
| B.人工合成的具有生命活性的蛋白质—结晶牛胰岛素,是1965年我国科学家最先合成的 |
| C.重金属盐能使蛋白质变性,所以误食重金属盐会中毒 |
| D.浓HNO3溅在皮肤上,使皮肤呈黄色,是由于浓HNO3和蛋白质发生颜色反应 |