关于原电池的叙述中正确的是
| A.构成原电池的电极是两种不同的金属 |
| B.原电池是将化学能转化为电能的装置 |
| C.原电池负极发生的电极反应是还原反应 |
D.原电池的正极是还原剂,总是溶液中的阳 离子在此被还原 离子在此被还原 |
下列有关金属防护的说法不正确的是
| A.通过镶嵌锌块保护船体的方法叫牺牲阳极的阴极保护法 |
| B.埋铁制管线时应选择致密、干燥的土壤层 |
| C.青铜器表面覆盖防渗高分子膜,可防止铜绿形成 |
| D.纯银器表面在空气中因电化学腐蚀渐渐变暗 |
用图所示装置除去含CN—、Cl—废水中的CN—时,控制溶液pH为9~10,阳极产生的ClO—将CN—氧化为两种无污染的气体,下列说法不正确的是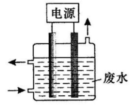
| A.用石墨作阳极,铁作阴极 |
| B.阳极的反应式为:Cl-+2OH- -2e-=ClO-+H2O |
| C.阴极的反应式为:2H2O+2e-=H2↑+2OH- |
| D.除去CN-的反应:2CN-+5ClO-+2H+=N2↑+2CO2↑+5Cl-+H2O |
微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示(质子交换膜只允许H+通过)。下列有关微生物电池的说法错误的是
| A.正极反应中有CO2生成 |
| B.微生物促进了反应中电子的转移 |
| C.质子通过交换膜从负极区移向正极区 |
| D.电池总反应为C6H12O6+6O2=6CO2+6H2O |
己知丙烷的燃烧热△H= -2215kJ·mol-1,若一定量的丙烷完全燃烧后生成1.8g水,则放出的热量约为
| A.55 kJ | B.220kJ | C.550 kJ | D.1108 kJ |
下列制作铅笔的材料与相应工业不对应的是
| A.橡皮擦——橡胶工业 |
| B.铝合金片——冶金工业 |
| C.铅笔芯——电镀工业 |
| D.铅笔漆—— 涂料工业 |