在下列各组溶液中,离子间一定能大量共存的是( )
A.pH=1的溶液:K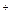 、Cu 、Cu 、Br 、Br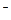 、SO 、SO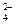 |
B.含有0.1 mol·L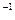 I I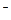 的溶液:NH 的溶液:NH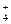 、Fe 、Fe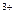 、SO 、SO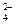 、Cl 、Cl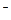 |
C.含有0.1 mol·L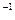 HCO HCO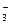 的溶液:Na 的溶液:Na 、Al 、Al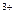 、NO 、NO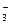 、OH 、OH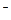 |
D.强酸性溶液:K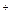 、Mg 、Mg 、NO 、NO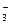 、ClO 、ClO |
将NaCl和NaBr的混合物a g溶于足量水中配成1 L溶液A,再向A中通入足量Cl2,充分反应后蒸发溶液至干得到(a-2) g晶体。则A溶液中Na+、Cl-、Br-的物质的量之比肯定不正确的是
| A.3∶1∶4 | B.3∶2∶1 | C.3∶1∶2 | D.4∶3∶1 |
标准状况下,将V L A气体(摩尔质量为Mg·mol-1)溶于0.1 L水中,所得溶液密度为ρ g·mL-1。则此溶液物质的量浓度为
A.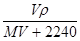 mol·L-1 mol·L-1 |
B.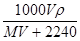 mol·L-1 mol·L-1 |
C.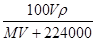 mol·L-1 mol·L-1 |
D.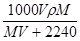 mol·L-1 mol·L-1 |
由钠和氧组成的某种离子晶体中阴离子只有O2-和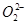 (过氧离子)。在此晶体中,氧元素和钠元素质量之比是48∶92,则其中O2-和
(过氧离子)。在此晶体中,氧元素和钠元素质量之比是48∶92,则其中O2-和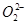 的物质的量之比为
的物质的量之比为
| A.2∶1 | B.1∶1 | C.1∶2 | D.1∶3 |
只给出下列甲中和乙中对应的量,不能组成一个求物质的量的公式的是
| ① |
② |
③ |
④ |
⑤ |
|
| 甲 |
物质粒子数 |
标准状况下气体摩尔体积 |
固体体积 |
溶质的质量分数 |
非标准状况下物质的质量 |
| 乙 |
阿伏加德罗常数 |
标准状况下气体体积 |
固体密度 |
溶液的体积 |
物质的摩尔质量 |
A.②③④ B.③④⑤ C.③④D.③
设NA表示阿伏加德罗常数值,下列说法正确的是
| A.1 L 1 mol·L-1 CH3COONa溶液中存在NA个CH3COO- |
| B.1 mol CnH2n+2含有(3n+1)NA个共价键 |
| C.1 mol Cl2参加化学反应获得的电子数都是2NA |
| D.1 mol NO2气体降温后颜色变浅,其所含的分子数仍为NA |